Användare:Knoppson/Elektroteknik
Denna bok är tänkt att sammanställa såväl som sammanfatta de allra flesta av Wikipedias artiklar om elektroteknik.
Introduktion
[redigera | redigera wikitext]Elektroteknik betyder i princip praktiska tillämpningar av fysikens lagar främst vad beträffar elektricitet och magnetism även om viss mekanik och optik nog också kan sägas ingå.
Elektron
[redigera | redigera wikitext]Elektron kallas den lilla partikel som cirkulerar runt alla atomer. Valenselektroner i metaller kan fås att vandra i enlighet med pålagd elektrisk fältstyrka, E, vars enhet är V/m.
Originalartikel
[redigera | redigera wikitext]
En elektron är en elementarpartikel med en negativ laddning (elementarladdning). Elektronen tillhör partikelgruppen leptoner. En atomkärna omgiven av elektroner bildar en atom. Elektroner är lätta partiklar; en proton är cirka 1 836 gånger tyngre än elektronen.
Elektronen har en elektrisk laddning på minus elementarladdningen (-1,6021765·10-19 coulomb) och en massa på 9,1093826·10-31 kg[1] (0,51 MeV/c2).[2] Elektronen tillhör familjen leptoner och har spinn +1/2 eller -1/2, och är alltså en fermion, det vill säga att den beskrivs i statistisk mekanik med Fermi-Dirac-statistik. Elektronens magnetiska dipolmoment är ungefär en promille större än Bohrmagnetonen.[3]
Elektronen betecknas ofta med symbolen e–. Antipartikeln till elektronen heter positron, vilken har samma egenskaper som elektronen men motsatt laddning.
Historia
[redigera | redigera wikitext]Begreppet elektron användes första gången 1871 i ett arbete av Wilhelm Eduard Weber om elektricitet i metaller, med betydelsen "elektrisk smådel". Begreppet fick dock ingen vidare användning, även om Hermann von Helmholtz 1881 införde en enhetsladdning för mängden elektricitet som en monovalent atom har enligt Faradays lag (Michael Faraday). 1897 upptäckte J J Thomson att elektronen var en subatomär partikel när han studerade katodstrålar. Om man antog att strålarnas partiklar hade samma ladding som monovalenta joner, visade avlänkningen i ett magnetfält att dess massa var ungefär 2 000 gånger mindre än väteatomens. I samma tid visade Pieter Zeeman och Hendrik Lorentz att partiklar med samma e/m-förhållande kunde förklara Zeemaneffekt i atomspektrum.
I början trodde flera forskare – bland dem Thomson – att elektronens massa endast var en effekt av dess elektrostatiska energi.[4] Genom att likställa coulombenergi och massa får man den klassiska elektronradien, som är lika med spridningslängden för Thomsonspridning, ungefär 10-15 m. Enligt kvantelektrodynamik är dock elektronen en punktpartikel.
2008 lyckades forskare för första gången filma en elektron[5].
Atomer och molekyler
[redigera | redigera wikitext]Elektroner i en atom kretsar kring atomkärnan. Elektronerna har vissa bestämda energivärden, ju mer energi en elektron har desto längre bort från kärnan med de positivt laddade protonerna befinner den sig. De elektroner som har samma energivärde befinner sig på samma energinivå, så kallade skal, i atomen.
Om en elektron tillförs extra energi hoppar den ett skal utåt, atomen är då exciterad. Det finns en maxgräns för hur mycket energi en elektron kan tillföras och ändå vara en del av en atom. Tillförs en elektron mer energi än maxgränsen så frigör den sig från atomen, varvid atomen blir en positivt laddad jon.
Elektricitet (del 1)
[redigera | redigera wikitext]Elektricitet, som ofta benämns elektrisk ström, orsakas av att laddade partiklar rör sig under inflytande av ett yttre elektriskt fält. Vanligen är de laddade partiklarna fria elektroner i en elektrisk ledare. Strömstyrka kan mätas med en galvanometer (amperemeter).
Statisk elektricitet beror på att ett objekt har ett överskott på laddningar. Om laddningarna är negativa, som elektroner, säger man att objektet är negativt laddat; annars är det positivt laddat. När det finns lika många negativa som positiva laddningar (protoner), sägs objektet vara elektriskt neutralt. Ett underskott av laddningar kan behandlas som ett överskott av motsatt laddning. Laddningsmängd mäts med elektrometer.
Kemi
[redigera | redigera wikitext]Kemi handlar i allt väsentligt om att studera hur elektroner i en atoms elektronskal utbyts med andra atomer. Man säger att ett visst atomslag har ett antal valenselektroner som kan lånas / delas / lånas ut, och denna process kallas kemisk reaktion, varvid nya molekyler och därmed ämnen byggs upp. Elektroner finns i atomer, där de befinner sig i atomskalen. Maximala antalet möjliga elektroner i skalen följer formeln (skalen har namn efter bokstäver med start från K, det vill säga skal 1 heter K, skal 2 heter L osv) detta betyder dock inte att skalen alltid kommer vara fyllda till sitt max då atomerna strävar efter att ha 8 valenselektroner.
Eftersom det är energimässigt gynnsamt att ha alla skal fyllda gör detta vissa föreningar mycket stabila. Till exempel är ädelgaserna, som har alla skal fyllda, väldigt obenägna till att ingå i kemiska föreningar, medan till exempel kol, syre och väte är betydligt mer benägna till detta.
Subatomär fysik
[redigera | redigera wikitext]Elektroner deltar också i de subatomära fysikens reaktioner. Välkänd är betasönderfall där i vissa fall en neutron i en atomkärna sönderfaller i en proton och en elektron. Fria neutroner råkar förr eller senare ut för samma öde ().
Referenser
[redigera | redigera wikitext]- ^ NIST (5 december 2007). ”Electron mass”. 2006 CODATA recommended values. http://physics.nist.gov/cgi-bin/cuu/Value?me.
- ^ NIST (5 december 2007). ”Electron mass energy equivalent in MeV”. 2006 CODATA recommended values. http://physics.nist.gov/cgi-bin/cuu/Value?mec2mev.
- ^ NIST (5 december 2007). ”Electron magnetic moment to Bohr magneton ratio”. 2006 CODATA recommended values. http://physics.nist.gov/cgi-bin/cuu/Value?muemsmub.
- ^ Elektron i Nordisk familjebok (andra upplagan, 1907)
- ^ Charlotta von Schultz. "Se elektronen bli filmstjärna". Ny tekniks nätupplaga, 22 februari 2008. Hämtad 22 februari 2008.
Antimateria/Antipartikel
[redigera | redigera wikitext]
Antipartiklar från höger uppifrån och ner: positron, antiproton, antineutron.
Antimateria är motsatsen till den vanliga materia, som vår galax och resten av vårt synliga universum består av (i detta sammanhang ibland kallad koinomateria för distinktionens skull). Det finns en antipartikel för varje vanlig partikel: till exempel protoner–antiprotoner, neutroner–antineutroner och elektroner–positroner. Vissa partiklar är sina egna antipartiklar, till exempel fotoner och Z-bosoner.
Teoretisk bakgrund
[redigera | redigera wikitext]Enligt standardmodellen, den gängse grundläggande beskrivningen av universum, finns tolv olika typer av materiapartiklar och fyra (kända) kraftbärande partiklar. Till dessa materiapartiklar och kraftbärande partiklar kopplas deras spegelbilder med avseende på vissa symmetrier. Till exempel har en antipartikel samma storlek på sin elektriska laddning som sin motsvarande partikel, men med omvänt tecken. I övrigt tror man att en partikel och motsvarande antipartikel är lika. Om olikheter finns mellan partiklar och antipartiklar kan detta påvisa vissa symmetribrott, till exempel CPT (charge conjugation, parity, time reversal, ”laddningskonjugering, paritet, tidsreversering”). Detta skulle i sin tur påvisa att de gängse fysikaliska teorierna har inneboende fel vad gäller fundamentala teoriers (som speciella relativitetsteorin) giltighet.
Enligt kvantfältteori skapas partiklar och deras motparter konstant hela tiden. Detta påverkar vår beskrivning av vakuum på ett direkt sätt. Något vakuum i klassisk mening finns sålunda inte, då det hela tiden skapas partikelpar. Livslängden för dessa par av partiklar och antipartiklar är dock mycket kort och bestäms av Heisenbergs obestämdhetsrelation i formeln
vilket betyder att energi kan lånas från ingenting under en kort tidsrymd.
Einsteins formel E=mc² (Energi = massa * ljusets hastighet i kvadrat) säger att det finns energi där det finns massa; all energi har (relativistisk) massa. En del av denna energi utvinns i dagens kärnkraftverk, genom att helt enkelt klyva atomer. Det finns dock teoretiskt mer effektiva sätt. När t ex anti-elektroner och elektroner kolliderar annihileras dessa och all massenergi omvandlas till rörelseenergi för fotoner. 100 % av massan blir alltså energi.
Historisk bakgrund och laboratorieresultat
[redigera | redigera wikitext]Antipartiklar postulerades först av Paul Dirac 1928, när han formulerade om Schrödingers vågekvation för att göra denna Lorentzinvariant. Dirac fann att då speciella relativitetsteorin och schrödingerekvationen stöptes samman uppstod två ekvivalenta lösningar så när som på ett minustecken. Dirac tolkade då den negativa lösningen som bevis för antipartiklar. Elektronens antipartikel påvisades några år senare av svenskamerikanen Carl D Anderson.
Länge såg man antimateria som något rent teoretiskt, men med Andersons upptäckt 1932 av positronen kom första beviset för att antimateria verkligen existerade. En positron är en elektron med motsatt laddning (det vill säga positiv). Antiprotonen och antineutronen upptäcktes 1955 av Emilio Segrè och Owen Chamberlain. Efter dessa upptäckter har existensen av antimateria verifierats mycket övertygande och produktionen av antimateria är idag något som rutinmässigt görs i till exempel partikelacceleratorer.
I CERN pågår experiment för att undersöka om en väteatom (en proton och en elektron) och dess antipartikel (en antiproton och en antielektron) har samma spektrum. Man lyckades 1995 producera ett tiotal antiväteatomer. Dessa existerade endast i 40 nanosekunder, vilket beror på att antimateria och materia annihilerar varandra när de får kontakt. Man kan alltså inte förvara antimateria på grund av detta, eftersom det inte får ha någon kontakt med materia alls. Det har forskargruppen på CERN löst genom att förvara antivätet svävande i en fälla av magnetfält och elektriska fält. Man har efter detta producerat stora mängder antiväte, och man vill undersöka dessa antiatomers spektrum för att se om de, som teorin förutsäger, har exakt samma spektrum.
Den 17 november 2010 publicerade Nature en artikel som beskrivet att ALPHA-gruppen blev de första i världen som lyckades att fånga antiväte-atomer via magnetiska fält.[1] Man lyckades fånga 38 atomer av antiväte för runt en sjättedels sekund.[1] Det var den första gången som neutral antimateria fångats.
Kosmologisk antimateria
[redigera | redigera wikitext]Förmodligen bildades lika mycket antimateria som materia vid den förmenta Big Bang, varefter det mesta av materian och antimaterian kolliderade och annihilerade varandra. Det måste dock ha funnits en mycket liten asymmetri, d.v.s. det måste ha funnits en aning mer materia än antimateria. Det är denna materia som är den materia vi idag kan se i universum. Om detta hade Klein-Alfvéns kosmologi en annan uppfattning. Frågan har förbryllat forskare länge, och är något som man fortfarande inte löst på ett tillfredsställande sätt.
Antipartiklar bildas varhelst i kosmos närhelst en kollision inträffar mellan högenergetiska partiklar. Detta händer i vår atmosfär, när kraftig kosmisk strålning tränger in. Man är inte säker på om antimateria i övrigt finns "naturligt" i universum. Om det fanns antimateria i någon region i universum, skulle man se resultatet genom intensiv strålning från annihilationer vid gränsen av antimateriaregionen, men någon sådan strålning har man ännu inte observerat vid genomförda ballongförsök. 1977 trodde man sig ha funnit ett moln av antimateria i Vintergatans mitt, men detta är inte verifierat.
Experimentell översikt
[redigera | redigera wikitext]Hittills utförda mätningar på utomjordiska källor har genomförts med stratosfärballonger i polartrakterna, som för upp sin nyttolast i form av detektorer till sådan höjd att observationer blir meningsfulla:
- 1994 CAPRI CE (Cosmic AntParticle Ring Imaging Experiment)
- 1993 BESS (Balloon-borne Experiment with Superconducting Spectrometer)
- 2004 BESS Polar
Till dessa försök kommer nu satellitburna experiment, där arbetet med detektorerna pågått flera år före uppskjutningen:
- 2005 - 2008 AMS (Alpha Magnetic Spectrometer)
- 2006 - 2009 PAMELA (Payload for Antimatter Matter Exploration and Light-nuclei Astrophysics) är ett internationellt samarbete om ett system av partikeldetektorer som avses placeras i en rysk Resurs DK-1 satellit. PAMELA sköts upp den 15 juni 2006 ifrån Kazakstan. Det primära målet för PAMELA är att mäta energispektra för antiprotoner och positroner i den kosmiska strålningen.
Referenser
[redigera | redigera wikitext]- ^ [a b] Andresen, G. B.; Ashkezari, M. D.; Baquero-Ruiz, M.; Bertsche, W.; Bowe, P. D.; Butler, E.; Cesar, C. L.; Chapman, S. et al. (2010). "Trapped antihydrogen". Nature. doi:10.1038/nature09610
Externa länkar
[redigera | redigera wikitext]Atom
[redigera | redigera wikitext]En atom, från grekiskans ἄτομος, átomos, vilket betyder "odelbar", är den minsta enheten av ett grundämne som definierar dess kemiska egenskaper. Namnet skapades eftersom den antika atomteorin såg atomen som odelbar, men sedan länge vet man att så inte är fallet.
En atom består av positivt laddade protoner, neutrala neutroner, samt negativt laddade elektroner. Protonerna och neutronerna befinner sig i atomkärnan och kallas sammantaget för nukleoner. Atomkärnan innehåller nästan all massa i atomen, då protoner och neutroner båda är cirka 1800 gånger tyngre än elektronerna. Elektronerna befinner sig i elektronmolnet som omger kärnan och detta elektronmoln är många gånger större än denna kärna. En atom är ungefär 0,1 nanometer (1 ångström) i diameter. Atomers massa mäts av praktiska skäl ofta i atommassenheten (u), som är ungefär 1,66·10−27 kg. Den lättaste atomen är väte, som väger cirka 1 u, vilket innebär att det går nära 6·1023 väteatomer på ett gram väte. De tyngsta atomerna som har studerats väger nära 300 u.
Antalet protoner i kärnan kallas atomnummer, och bestämmer vilket grundämne det rör sig om. Den enklaste atomen är väte som har atomnummer ett och består av en proton och en elektron.
Antalet nukleoner, protoner plus neutroner, kallas masstal. Atomer med samma atomnummer men olika masstal kallas isotoper. Deuterium är en isotop av väte med masstalet två, och består av en proton, en neutron (totalt två nukleoner) och en elektron. Antalet elektroner i en atom är lika med antalet protoner, så totalt sett är atomen oladdad. Om en atom får fler eller färre elektroner blir den en jon, som är elektriskt laddad.
Atomer kan även förekomma i jongitter. När atomer joniseras och därefter bildar ett salt så ser det där saltet ut på ett särskilt sätt. Det har bildats ett jongitter bestående av olika atomer och det brukar visa hur atomerna sitter i saltet.
Atomens fysik
[redigera | redigera wikitext]Atomens fysik studeras på två olika plan: dels kvantmekaniskt, där elektronerna och deras rörelser är i fokus, och dels i den subatomära fysiken, där främst kärnan är i fokus.
Elektroner
[redigera | redigera wikitext]Man kan via kvantmekanik och med hjälp av pauliprincipen visa att varje elektron kommer att befinna sig i ett av flera "skal" eller "band". Till skillnad mot vad många enklare illustrationer ger sken av (som till exempel modellen av en heliumatom ovan) cirkulerar inte elektronerna snällt kring kärnan likt planeterna i ett solsystem. Istället far elektronen omkring på ett oförutsägbart sätt som dock kan beskrivas med hjälp av en vågfunktion, som dock har ett sådant utseende att man kan hitta ett begränsat område där elektronen befinner sig med hög sannolikhet vid en viss tidpunkt. På grund av pauliprincipen kan varje sådant tillstånd endast upptas av två elektroner med olika spinn, men då flera tillstånd liknar varandra har de samma sannolikhetsmaxima, och de områden där dessa inträffar kallas elektronskal. Elektroner med samma energi kommer att vara i samma "skal". De elektroner med högst energi kommer att vara längst ifrån kärnan, de med minst energi närmast. Det skal med högst energi som innehåller elektroner i atomens grundtillstånd kallas valensskal, och de elektroner som ingår i detta kallas valenselektroner.
Elektroner kan även exciteras upp till skal med högre energi. När de sedan faller tillbaka utsänder de elektromagnetisk strålning i form av en foton. Om denna har en frekvens i den synliga delen av spektrumet upplever vi att ämnet har denna färg.
Kärnan
[redigera | redigera wikitext]Antalet protoner och/eller neutroner kan förändras via fission, fusion eller radioaktivt sönderfall, och atomen övergår då i en eller flera nya atomer.
För ett grundämne gäller att antalet protoner är konstant men antalet neutroner kan variera. Till exempel klor har 17 protoner i kärnan men har stabila isotoper med 18 och 20 neutroner. Ett annat exempel är väte med en proton i kärnan samt 0, 1 eller 2 neutroner, där de olika varianterna begåvats med egna namn: protium, deuterium respektive tritium.
Kemi
[redigera | redigera wikitext]Kemiska reaktioner beror på att atomer utbyter elektroner med varandra. En självständig atom har lika många elektroner som protoner, så att den är elektriskt neutral. För ädelgaserna är detta tillstånd stabilt och dessa är också mycket obenägna att reagera kemiskt.
För övriga atomslag kan energiinnehållet minskas om atomen får 'låna' eller 'låna ut' en elektron till en granne, och naturen strävar efter så lågt energiinnehåll som möjligt; jämför en boll som gärna vill rulla ner i botten av ett hål. Således är till exempel Natrium mycket benäget låna ut en elektron, och Klor mycket benägen låna en, varför NaCl är en stabil kemisk förening bestående av två atomslag.
Helt avgörande för de kemiska egenskaperna är antalet valenselektroner för atomslaget. Detta beror endast på atomnummer, varför olika isotoper av ett ämne i princip har samma kemiska egenskaper.
I lösningar är det vanligt att atomer lånat ut/lånat en elektron, och ändå inte har något fast föhållande till låntagaren/givaren. Atomen är då laddad och kallas jon. En sådan lösning leder elektricitet.
Optik
[redigera | redigera wikitext]Optik behandlar ljus, som uppstår av förändringar i elektronernas energi. Exempelvis kan man värma ett ämne, varvid elektronerna rör sig livligare och livligare. Men de strävar efter att återta sina lägre energiniåver; när detta sker avges en foton vars våglängd bestäms av ämnets möjliga energinåver. Olika våglängder uppfattar vårt öga som färg, varför vi säger att olika ämnen har olika färg.
Historik
[redigera | redigera wikitext]Filosofiska funderingar om atomer återfinns i antikens Grekland och hos indierna på 400- och 500-talen f.Kr. Det var grekerna som gav atomen sitt namn, efter det grekiska ordet atomos, som betyder "odelbar".
De tidigaste kända idéerna om något som liknar atomer utvecklades av Demokritos i Grekland runt 450 f.Kr. Idén dök inte upp igen förrän under renässansen.
År 1803 använde John Dalton konceptet. Han lade fram en teori om att alla grundämnen består av atomer av ett enda, unikt slag, och att dessa atomer kunde slås samman och forma kemiska föreningar.
År 1897 upptäckte J.J. Thomson elektronen, vilket motbevisade konceptet att atomer är odelbara. Thomson upptäckte senare även förekomsten av isotoper.
Thomson trodde att elektronerna var jämnt fördelade i atomen, balanserade av en oföränderlig sjö av positiv laddning. Detta kallas Thomsons atommodell och visade sig emellertid vara felaktigt. Detta menade Ernest Rutherford då han 1909 lade fram teorin att en atoms positiva laddning, och större delen av dess massa, återfinns i mitten av atomen, i kärnan, och att elektronernas är mindre partiklar som rör sig likt planeter runt en stjärna. År 1913 lade Niels Bohr fram sin kvantfysiska teori, som sade att elektronernas omloppsbana var bestämd och orubblig.
År 1926 hävdade Erwin Schrödinger att elektroner inte beter sig som partiklar utan som vågor. En konsekvens av detta, påpekade Werner Heisenberg ett år senare, är att det är matematiskt omöjligt att finna exakta värden för både positionen och rörelsen av en partikel vid en specifik tidpunkt. Istället kunde man hitta ett antal möjliga värden för dess rörelse, för en angiven position, och tvärtom. Således övergavs de tidigare modellen av en atom, och istället menades det att en elektron har ett visst område inom vilket den är mest sannolik att befinna sig, beskrivet med hjälp av en vågfunktion.
Se även
[redigera | redigera wikitext]- Grundämne
- Niels Bohrs atommodell
- Kvantmekanik
- Periodiska systemet
- Demokritos
- Ernest Rutherford
- John Dalton
- Niels Bohr
Externa länkar
[redigera | redigera wikitext]![]() Wikimedia Commons har media som rör Knoppson/Elektroteknik.
Wikimedia Commons har media som rör Knoppson/Elektroteknik.
Atomkärna
[redigera | redigera wikitext]
Atomkärna, en samling av neutroner och protoner som sitter ihop. Bildar tillsammans med elektroner en atom. Antalet protoner i kärnan bestämmer vilket grundämne och antalet neutroner vilken isotop som atomen utgör. Väteatomkärnan är den enklaste, bestående av endast en proton.
Partiklarna i atomkärnan hålls samman av den starka kärnkraften.
Se även
[redigera | redigera wikitext]Betasönderfall
[redigera | redigera wikitext]Betasönderfall eller β-sönderfall är (tillsammans med alfasönderfall) en av två huvudtyper av sönderfall hos atomkärnor. Betasönderfall sker genom svag växelverkan. Vid betasönderfall förblir antalet nukleoner (protoner och neutroner) konstant, medan däremot fördelningen mellan protonerna och neutronerna ändras. Med andra ord är masstalet (A) konstant medan atomnumret (Z) ändras. Betasönderfall kan delas in i tre undertyper:
- Beta minus-sönderfall (eller β−-sönderfall): En neutron sönderfaller i en proton som stannar kvar i kärnan, en elektron som har såpass hög energi att atomen inte orkar hålla kvar den och i en neutrino (i detta fall en antineutrino).
- Beta plus-sönderfall (eller β+-sönderfall): En proton faller sönder i en neutron, en positron (en "anti-elektron") och en neutrino.
- Elektroninfångning: En proton "fångar" in en elektron, och bildar en neutron, samtidigt som den sänder ut en neutrino. Detta sker främst om energin som skulle frigöras av ett beta plus-sönderfall inte är tillräcklig för att skapa en elektron.
De elektroner som sänds ut vid β−- och β+-sönderfall kallas betapartiklar och utgör betastrålning.
β−-sönderfall
[redigera | redigera wikitext]

En neutron i atomkärnan sönderfaller i en proton, en elektron, och en antineutrino,
Eftersom det bildas en proton i sönderfallet är atomnumret hos dotterkärnan ett högre än atomnumret hos den ursprungliga kärnan.
Betasönderfall sker genom svag växelverkan. På elementarpartikelnivå är β− sönderfall en omvandling av en nerkvark till en uppkvark genom utsändande av en W−-boson som sönderfaller i en elektron och en elektronantineutrino.
Sidoeffekter
[redigera | redigera wikitext]Vid sönderfallet kan dotterkärnan hamna i ett exciterat tillstånd för att sedan sända ut energiöverskottet som gammastrålning. Även de inre elektronskalen exciteras som kan ge upphov till röntgenstrålning, s.k. karakteristisk röntgen på väg tillbaka till grundtillståndet. Energiöverskottet kan även tas upp av en annan elektron som avges som en s.k. augerelektron, som har mycket lägre energier än betastrålning.
Farlighet
[redigera | redigera wikitext]Betapartiklar med en energi på 2 MeV har en räckvidd på ungefär en centimeter i vävnad och 10 meter i luft. Betastrålning kan enkelt skärmas med plåt eller glasrutor, men för gammastrålningen som bildas i samband med betasönderfall behövs det tyngre avskärmning.
T.ex i ett kärnkraftverk utsätts arbetarna för betastrålning i princip enbart under arbete inuti locket till reaktorn. Där har neutronerna från kärnklyvningarna aktiverat stålet till olika radioaktiva isotoper som sänder ut betastrålning. Denna går dock att skydda sig enkelt ifrån genom att använda skyddsglasögon och en extra overall eller heltäckande gasmask eftersom det ibland även finns luftkontamination. Gammastrålningen finns det generellt ingen personlig skyddsutrustning för på kärnkraftverk utan den minimeras genom fasta installationer.
Andra typer av radioaktivt sönderfall
[redigera | redigera wikitext]
| ||||||||||||||||
Bohrmagnetonen
[redigera | redigera wikitext]Bohrmagnetonen (efter Niels Bohr) är ett mått på det magnetiska moment som en elektron med rörelsemängdsmoment , där är Diracs konstant, ger upphov till. Bohrmagnetonen betecknas med μB, vilket tyvärr gör att den riskeras att förväxlas med den magnetiska konstanten eller permeabiliteten. Uttrycket för Bohrmagnetonen är
där e är elementarladdningen och m0 elektronens massa.
Värdet härleddes först ur Bohrs atommodell, där elektronen antogs gå runt en atomkärna i en cirkelbana och där denna ringström av laddning skulle ge upphov till ett magnetiskt moment. Dess storleksordning stämde väl överens med magnetiseringen av magnetiska material. Senare visade det sig att magnetism mest härstammar från elektronernas spinn som ger ett inneboende magnetiska moment. Värdet är bara någon promille större än bohrmagnetonen.
Källor
[redigera | redigera wikitext]- NIST (5 december 2007). ”Bohr magneton”. 2006 CODATA recommended values. http://physics.nist.gov/cgi-bin/cuu/Value?mub.
- NIST (5 december 2007). ”Bohr magneton in eV/T”. 2006 CODATA recommended values. http://physics.nist.gov/cgi-bin/cuu/Value?mubev.
- Haken, H. & Wolf, H.C. (2000). The Physics of Atoms and Quanta. Springer-Verlag. ISBN 3-540-67274-5
Coulomb
[redigera | redigera wikitext]Coulomb (C), (svenskt uttal /kulɔ´mb/), är SI-enheten för elektrisk laddning och definieras utifrån ampere. 1 coulomb är laddningen som under 1 sekund passerar genom en ledare där strömstyrkan är 1 ampere. Det motsvarar ungefär laddningen av 6,24·1018 elektroner. Enheten är uppkallad efter Charles de Coulomb (1736–1806).
Se även
[redigera | redigera wikitext]Elektricitet (del 2)
[redigera | redigera wikitext]

Elektricitet är ett fysikaliskt fenomen. Grunden till elektricitet är att materia kan ha en elektrisk laddning. Fenomenet tar sig uttryck i välkända former som blixtar och statisk elektricitet liksom i elektromagnetiska fält och elektromagnetisk induktion. Ordet elektricitet kommer av det grekiska ordet för bärnsten, ηλεκτρον (elektron) och slutligen från latinets ēlectricus (bärnstensliknande). Ordet myntades av britten William Gilbert år 1600 vid hans experiment med statisk elektricitet.
I dagligt tal räcker ordet elektricitet för att beskriva ett antal fysikaliska effekter. I vetenskaplig terminologi är däremot denna term vag, och det är bättre att tala om följande inbördes relaterade men distinkta fenomen:
- Elektrisk laddning — en egenskap hos vissa subatomära partiklar och som bestämmer deras elektromagnetiska interaktioner. Elektriskt laddad materia både skapar och påverkas av elektromagnetiska fält.
- Elektrisk ström — en rörelse eller flöde av elektriskt laddade partiklar, som vanligen mäts i ampere.
- Elektromagnetiskt fält — ett kraftfält som skapas av en elektrisk laddning på laddningar i dess närhet.
- Elektrisk potential — förmågan hos ett elektriskt fält att utföra arbete, vilket vanligen mäts i volt.
- Elektromagnetism — en grundläggande interaktion mellan magnetfältet och närvaron och rörelsen hos en elektrisk laddning.
Elektriska fenomen har studerats sedan antiken, även om vetenskapliga framsteg inom området inte gjordes innan 16- och 1700-talen. Praktiska användningsområden för elektriciteten förblev dock få tills dess att ingenjörer under det senare 1800-talet lärde sig att använda elektricitet i hem och inom industrin. Den snabba expansionen av elektrisk teknik vid den transformerade samhället i grunden. Elektricitetens ovanliga flexibilitet som energikälla betyder att den kan användas i en rad sammanhang, inklusive för transport, uppvärmning, ljus, kommunikation och beräkning. Elektriciteten kan förväntas utgöra ryggraden hos det industriella samhället över en överskådlig framtid.[1]
Historia
[redigera | redigera wikitext]
För några få generationer sedan använde man inte elektricitet. Gatlamporna var gaslampor, transportmedlet var häst & vagn och maten kokades på vedspisar. På den tiden visste man knappt vad elektricitet var. Idag är vi helt beroende av elektriciteten; vi använder den i princip jämt.
Statisk elektricitet var känd redan under antiken. Under 600-talet f Kr upptäckte grekerna att om man gnuggade päls mot bärnsten, så kunde bärnstenen dra till sig lätta föremål. Efterhand upptäckte man flera andra ämnen med samma egenskap. Den första som studerade detta mer ingående var den engelska fysikern William Gilbert (1544–1603). Han kallade attraktionen som bildades för elektrisk kraft efter det grekiska ordet elektron, som betyder just bärnsten.
Idag förklarar vi elektriska fenomen med begreppet elektrisk laddning. Fransmannen Charles Dufay (1698–1739) var den första som visade att det finns två sorts laddningar, men det var Benjamin Franklin som införde begreppet positiv och negativ laddning. Omkring 1820 upptäckte Hans Christian Ørsted elektromagnetismen, för vilken André-Marie Ampère omgående formulerade matematiska ekvationer. Detta ledde till ökad experimentell aktivitet bland forskare under 1800-talet.
På 1900-talet blev det klart att positiv laddning är knuten till protonen och negativ laddning till elektronen.
Teori
[redigera | redigera wikitext]Man brukar beskriva elektricitet med klassisk elektrodynamik. Enligt denna teori består elektricitet av rörliga laddningar, som kan vara positiva eller negativa. Lika laddningar stöter bort - repellerar - varandra, medan olika laddningar drar till sig - attraherar - varandra. Om positiva och negativa laddningar finns på samma plats förintar de varandra i en elektrostatisk urladdning. Laddningarna påverkas också av material - material delas vanligen in i elektriska ledare, där laddningarna kan röra sig och på så sätt bilda en elektrisk ström, och isolatorer, som laddningarna inte kan röra sig genom.
En elektrisk ström räknas som positiv till sin riktning för ett flöde av positivt laddade partiklar från en punkt med högre elektrisk potential (spänning) till en punkt med lägre elektrisk potential. Strömstyrka kan bestämmas av potentialskillnaden mellan punkterna (spänningsfall som räknas i volt) och motståndet mellan dem (resistans om strömmen är likström, men impedans om strömmen är växelström). Vid likström kan strömstyrkan räknas ut med formeln (där I är ström, U spänning och R resistans. Om strömmen periodiskt växlar riktning (växelström) blir formeln (där Z är impedans).
Elektrisk laddning
[redigera | redigera wikitext]
Elektrisk laddning eller elmängd[2] (Q, q) är den fysikaliska storhet som påverkas av elektromagnetisk växelverkan, en av de fyra fundamentala krafterna. I Coulombs lag har laddning samma roll som massa i Newtons gravitationslag, men skillnaden är att laddning förekommer i två varianter, positiv och negativ.
Att det finns två och endast två typer av statisk elektricitet har varit känt sedan 1700-talet. Du Fay myntade termerna vitreös och resinös, för "glaselektricitet" och "kådaelektricitet".[3] Laddningar av samma typ repellerar varandra, medan växelverkan mellan laddningar av olika typ är attraktiv. Benjamin Franklin upptäckte att man kunde betrakta dessa som positiva och negativa laddingar, vars algebraiska summa är konserverad. Detta betyder att den totala laddning varken kan förnyas eller förintas, vilket gör den till en av de elementära egenskaper materia besitter.
Elektrisk laddning kvantifieras till negativa eller positiva multipler av elementarladdningen e.
Elektrisk ström
[redigera | redigera wikitext]
Elektrisk ström uppstår då en elektrisk laddning förflyttas. Ström definieras som laddning per tidsenhet. De laddade partiklarna är vanligtvis elektroner men kan även vara joner. I en elektrisk krets säger man av historiska skäl att strömmen går från högre till lägre potential även om elektronerna rör sig i motsatt riktning.
Elektriskt fält
[redigera | redigera wikitext]
Ett elektriskt fält är ett vektorfält som beskriver skillnader i den elektriska potentialen i rummet. Det kan beskrivas med "pilar" i rummet, som pekar från positiva laddningar till negativa. Elektriska fält påverkar andra laddningar med en kraft. Man kan också, kanske mer korrekt, säga att det elektriska fältet medierar kraftverkan mellan laddade föremål. Konceptet elektriskt fält introducerades av Michael Faraday.
Den elektriska fältstyrkan är en vektor med SI-enheten newton per coulomb (N C-1), eller om man så vill (och helt ekvivalent), volt per meter (V m-1). Riktningen för fältet i en given punkt definieras som riktningen på den kraft som fås på en positiv testladdning i punkten. Beloppet av fältet definieras som kvoten mellan kraftens belopp och laddningens storlek. Ett elektriskt fält innehåller elektrisk energi, med en energitäthet proportionell mot kvadraten på fältstyrkan. I en ofta använd analogi mellan elektriska och mekaniska storheter kan man säga att det elektriska fältet är för laddning vad acceleration är för massa och krafttäthet är för volym.
En laddning i rörelse omger sig inte bara med ett elektriskt fält, utan även med ett magnetiskt fält, och i en allmännare teori är dessa två fält inte längre separata fenomen – vad en observatör uppfattar som ett elektriskt fält kan en observatör i ett annat referenssystem uppfatta som en blandning av elektriska och magnetiska fält. Därför talar man inom fysiken ofta om ”elektromagnetism” och ”elektromagnetiska fält”. Inom kvantelektrodynamiken benämns det elektromagnetiska fältkvantat foton, en elementarpartikel med kvantiserad energi.
Elektrisk spänning
[redigera | redigera wikitext]
Elektrisk spänning är en skillnad i elektrisk potential mellan två punkter. Om punkterna skulle komma i kontakt med varandra genom en elektrisk ledare som till exempel en metalltråd eller resistor, uppstår en elektrisk ström som strävar att utjämna potentialskillnaden mellan punkterna. Strömmen består av en förflyttning av laddade partiklar, vanligtvis elektroner. En sammankoppling som praktiskt taget saknar motstånd kallas kortslutning.
Elektrisk spänning mäts i SI-enheten volt som förkortas V. Eftersom 1 V = 1 J/As, är elektrisk spänning den energi som laddningen 1 As avger eller upptar när den rör sig genom ett elektriskt fält. Enheten volt är ingen grundenhet i SI utan definieras som den spänning som krävs över till exempel en resistans för att strömstyrkan 1 A ska generera effekten 1 W enligt effektformeln effekt = spänning • ström. En storhet som anger den elektriska spänningen mellan två punkter brukar betecknas U (av ty. Unterschied som betyder 'differens', 'skillnad'). Ett exempel är Ohms lag U=R • I som ger oss sambandet mellan spänningen, resistansen i sammankopplingen och styrkan hos den ström som därvid uppstår.
Elektromagnetism
[redigera | redigera wikitext]Varje elektriskt laddat föremål omges av ett elektriskt fält. I varje punkt har fältet en viss styrka, och en viss riktning. När ett elektriskt laddat föremål placeras i ett elektriskt fält, påverkas det av en elektrisk kraft, som är proportionell dels mot styrkan av fältet, dels mot den egna laddningen. När ett elektriskt laddat föremål rör sig genom ett elektriskt fält, påverkas det av en magnetisk kraft.
Elektrisk laddning och magnetism är två sidor av samma kraft, elektromagnetism. Enkelt uttryckt är elektromagnetism det som uppstår ur att en foton växelverkar med en laddad partikel. Varje rörelse av elektriska laddningar ger upphov till ett magnetfält, och varje magnetfält påverkar elektriska laddningar att röra sig. Den fundamentala kraften förmedlas av fotoner och växelverkar med alla laddade partiklar. Den elektromagnetiska kraften ligger bakom i princip alla fenomen i vår vardag som inte orsakas av gravitationen. Den skapar bland annat kemiska bindningar, normalkrafter (som hindrar föremål från att flyta in i varandra), friktion och ytspänning.
Elektricitet som naturfenomen
[redigera | redigera wikitext]Elektriska spänningar och urladdningar uppstår på många håll i naturen. Urladdningar i atmosfären kallas åska. Elektricitet spelar även stor roll i levande organismer, se bioelektricitet.
Elektroteknik
[redigera | redigera wikitext]
Den industrialiserade delen av världen är fullständigt präglad av elektrotekniska system. Några former av detta är elkraftteknik och elektronik.
Elkraftteknik
[redigera | redigera wikitext]Användning
[redigera | redigera wikitext]Elektricitet används bland annat för uppvärmning, kylning, belysning och motorer. Elektriciteten har kemiska verkningar vid elektrolys av ämnen i vätska.
Produktion
[redigera | redigera wikitext]
Elektrisk energi omvandlas av andra energiformer. En generator använder rörelseenergi. En solcell använder ljus. En bränslecell använder kemisk energi. Elektricitet produceras vanligen i kraftverk, till exempel kärnkraftverk eller vattenkraftverk.
Överföring
[redigera | redigera wikitext]Elöverföring, det vill säga överföring av elektrisk energi långa sträckor, sker med högspänningsledningar. Eldistribution är överföring av el till hushåll.
Se kraftledning och transformator.
Handel med elektricitet
[redigera | redigera wikitext]Då trygg försörjning av elkraft är en förutsättning för ett modernt samhälle och då ingen kan garantera problemfri leverans uppstår ett behov av att skapa ett gemensamt elnät som kopplar samman alla producenter och konsumenter i ett större område. I Skandinavien samordnas elhandeln via en elbörs som kallas Nordpool. Det man sätter ett pris på är elektrisk energi, vanligtvis i enheten kilowattimme. Sverige har haft ett enhetligt pris över hela landet som givit ett förhållandevis lågt pris trots att tillgången av elkraft jämfört med efterfrågan kan ha stora kraftiga skillnader från plats till plats. Från och med 2011 vill man införa olika zon-indelningar i Sverige för att skapa ett mer rättvist elpris baserat på tillgång och efterfrågan. Zon-indelningen har föreslagits av EU med inrådan från övriga nordiska länder som tycker att svenska elmarknaden haft för stor fördel i handeln mellan länder. [4]
Skador av elektricitet
[redigera | redigera wikitext]Det är farligt att få elektriska strömmar genom kroppen. Strömstyrkor på knappt 1 milliampere brukar kunna förnimmas som kittlande, och strömmar över cirka 10 mA ger kramp i muskler som inte kan hävas förrän strömmen bryts. Spänningar som överstiger klenspänning anses vara farliga. Elektrisk ström kan dessutom ge brännskador.
Det finns flera viktiga faktorer för hur kroppen påverkas när en elektrisk ström passerar igenom den:
- Vilka kroppsdelar som blir utsatta
- Tiden man blir utsatt för strömmen.
- Storleken på strömstyrkan (vilket beror på spänningen och hur fuktig man är)
- Hur den elektriska strömmen passerar igenom kroppen.
- Vågform beroende om det är lik- eller växelström och i det senare fallet växelströmmens frekvens.
Farligast är om strömmen passerar thorax och hjärtat (till exempel genom att man med ena handen rör ett strömförande föremål och med den andra en jordad diskbänk). Kramper i hjärtat leder till hjärtflimmer eller hjärtstillestånd. Flimmer uppstår vid några tiotals milliampere, stillestånd vid något hundratal eller mer.[5]
Skadeverkan avtar vid högre frekvenser, vid 10 kilohertz har känseltröskeln ökat till den tiodubbla, och strömmar på 1 ampere vid 1 megahertz kan passera utan att man känner något eller får skador. Detta utnyttjas bland annat vid elektrokirurgi där den värme som utvecklas får blodet att koagulera.[5]
Se även
[redigera | redigera wikitext]- Elektronik
- Elektromagnetism
- Statisk elektricitet
- Elektricitetens historia i Sverige
- Elektricitet i Stockholm
Litteratur
[redigera | redigera wikitext]- Elektricitet : historien om universums mäktigaste kraft av David Bodanis, övers. av Margareta Eklöf (2005), ISBN 91-1-301100-6, ISBN 91-7232-024-9. Översättning från The Electric Universe. The Shocking True Story of Electricity. 2005 ISBN 0-7393-1325-8 Random House, 2005.
Referenser
[redigera | redigera wikitext]- ^ Jones, D.A., ”Electrical engineering: the backbone of society”, Proceedings of the IEE: Science, Measurement and Technology 138 (1): 1–10
- ^ Svenska Elektriska Kommissionen (1988). ”Elektricitet och magnetism (1971)”. SI måttenheter: Storheter och enheter. Stockholm: Swedish Standards Institute
- ^ Charles François de Cisternay du Fay (5 december 1734). ”A Discourse concerning Electricity”. Philosophical Transactions. http://www.sparkmuseum.com/BOOK_DUFAY.HTM.
- ^ "Alexander Norman". ”Nya prisområden kan ge dyrare elpris”. Nya prisområden kan ge dyrare elpris. http://www.el.nu/2010/10/nya-prisomraden-kan-ge-dyr-el-i-soder-och-billig-i-norr/. Läst 17 oktober 2010.
- ^ [a b] Wobschall, D. Circuit Design for Electronic Instrumentation. McGraw-Hill. 1987. Sid. 157f.
Elektrisk ström
[redigera | redigera wikitext]
Elektrisk ström uppstår då elektrisk laddning förflyttas. Ström definieras som laddning per tidsenhet. Den elektriska laddningen i form av partiklar är vanligtvis elektroner men kan även vara joner.
Upphovet till en ström är vanligtvis en spänning, det vill säga en skillnad i potential mellan två punkter. I en elektrisk krets anses strömmen gå från högre till lägre potential, alltså från plus till minus. Det bygger på den äldre föreställningen att det är positiva laddningar som strömmar. När man upptäckte elektronen, insåg man att strömmen i en ledning i själva verket består av minusladdade elektroner som rör sig åt andra hållet (från minus till plus). Båda modellerna förklarar lika bra hur strömmen strävar att utjämna potentialskillnader och därmed hur elektriska kretsar beter sig. Därför har man behållit den gamla konventionen att ange strömriktningen från plus till minus.
SI-enheten för elektrisk ström (elektrisk strömstyrka) är ampere med symbolen A, och är en av de sju grundenheterna. I fysikaliska formler används symbolen I (ty. Intensität 'styrka', 'intensitet') för elektrisk ström.
Strömtyper
[redigera | redigera wikitext]
Det finns olika typer av ström, oftast talar man om likström och växelström.
Se även
[redigera | redigera wikitext]Elektrometer
[redigera | redigera wikitext]Elektrometer, elektriskt instrument som används för att mäta elektrisk laddning och elektrisk potentialskillnad. Namnet används för flera olika typer av instrument.
- Det tidiga 1800-talets elektrometrar, också kallade elektroskop, baserades på kraftverkan mellan elektriska laddningar. Mekanismen vidareutvecklades under 1800-talet till "elektrostatiska voltmetrar" med visare och graderad skala.
- Modernare former av elektrometrar innehåller en förstärkare byggd med specialutvecklade elektronrör eller halvledarkretsar och med extremt hög ingångsresistans. Med dessa kan man indikera så låga strömmar som någon femtoampere, fA, 10-15 ampere. En sådan strömmätarkrets, kompletterad med några ytterligare komponenter, kan användas som mätinstrument för låga spänningar (millivolt) och laddningar (femtocoulomb) samt för höga resistanser (1000 teraohm, 1015 Ω, 1 petaohm, 1 PΩ ).
- En femtoampere motsvarar omkring 4000 elektroner per sekund. Den strömmen är så ringa att slumpbeteendet hos varje enstaka ledningselektron bidrar till en observerbar och oundviklig fluktuation i strömmen, brus, vilket sätter en gräns för vad som är möjligt att mäta.
Se även Elektrostatik
Elektronskal
[redigera | redigera wikitext]Elektronkonfiguration anger hur elektronerna i ett grundämnes atomer är arrangerade. Konfigurationen styr ämnets fysiska och kemiska egenskaper och bestämmer vilken grupp och period i det periodiska systemet ämnet inplaceras.
Eftersom elektroner är fermioner följer de Pauli-principen, som säger att två fermioner inte samtidigt kan befinna sig i samma kvantmekaniska tillstånd. Detta medför att allt eftersom fler elektroner tillkommer runt atomkärnan så måste de hamna i nya tillstånd som inte ännu är upptagna av redan närvarande elektroner.
Ett annat namn på dessa kvanttillstånd är orbitaler, efter engelskans orbit, (=kretsa, bana). En lite missvisande men traditionellt använd bild för att beskriva dessa orbitaler, är att säga att elektronerna successivt fylls på i olika elektronskal som i sin tur byggs upp av underskal, och när ett skal eller underskal är fullt så påbörjas ett nytt.
Mer formellt så utgör de olika positionerna i elektronskalen stationära tillstånd i elektronens vågfunktion som bestäms av fyra så kallade kvanttal:
- Det första kvanttalet, n, anger elektronens energinivå och styr dess avstånd från kärnan. Detta motsvarar de traditionella "elektronskalen" (K, L, M, o.s.v.).
- Det andra kvanttalet, l, anger elektronens rörelsemängdsmoment och styr orbitalens excentricitet. l kan anta värden mellan 0 och n-1. Detta motsvarar "delskalet" och brukar traditionellt betecknas med en bokstav enligt nedanstående tabell snarare än ett tal:
| l-värde | bokstav |
|---|---|
| 0 | s |
| 1 | p |
| 2 | d |
| 3 | f |
| 4 | g |
- Det tredje s.k. magnetiska kvanttalet ml kan anta heltalsvärden mellan -l och +l.
- Det fjärde kvanttalet ms anger elektronens spinn och kan ha värdet -1/2 eller +1/2.
För varje värde på l kan en elektron därför anta 2(2l+1) tillstånd beroende på de övriga två kvanttalen ml och ms. Följande tabell visar de olika kombinationer med värden på ml och ms som är möjliga för olika värden på n och l:
| n-värde | l-värde/bokstav | ml och ms | Benämning |
|---|---|---|---|
| 1 | 0 / s | 0 och -1/2, +1/2 | 1s (2st) |
| 2 | 0 / s | 0 och -1/2, +1/2 | 2s (2st) |
| 1 / p | -1,0,1 och -1/2, +1/2 | 2p (6st) | |
| 3 | 0 / s | 0 och -1/2, +1/2 | 3s (2st) |
| 1 / p | -1,0,1 och -1/2, +1/2 | 3p (6st) | |
| 2 / d | -2,-1,0,1,2 och -1/2, +1/2 | 3d (10st) | |
| 4 | 0 / s | 0 och -1/2, +1/2 | 4s (2st) |
| 1 / p | -1,0,1 och -1/2, +1/2 | 4p (6st) | |
| 2 / d | -2,-1,0,1,2 och -1/2, +1/2 | 4d (10st) | |
| 3 / f | -3,-2,-1,0,1,2,3 och -1/2, +1/2 | 4f (14st) | |
| 5 | 0 / s | 0 och -1/2, +1/2 | 5s (2st) |
| 1 / p | -1,0,1 och -1/2, +1/2 | 5p (6st) | |
| 2 / d | -2,-1,0,1,2 och -1/2, +1/2 | 5d (10st) | |
| 3 / f | -3,-2,-1,0,1,2,3 och -1/2, +1/2 | 5f (14st) | |
| 4 / g | -4,-3,-2,-1,0,1,2,3,4 och -1/2, +1/2 | 5g (18st) |
Ovanstående tabell visar bara de möjliga kombinationerna, inte den ordning i vilken elektronerna successivt fyller olika tillstånd. Denna ordning styrs av tillståndens energinivå - de som har lägre energinivå fylls före de med högre energinivå. Följande uppställning (som läses radvis uppifrån och ned) visar detta. Observera att exempelvis 6s tillstånden har lägre energinivå än både 4f och 5d och därför fylls före dessa.
1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s 5f 6d 7p 8s 5g 6f 7d 8p ...
Ordningen är en teoretisk modell, den faktiska ordningen avviker något. Till exempel har nickel två 4s-elektroner och åtta 3d-elektroner, medan nästa ämne i ordningen, koppar bara har en 4s-elektron och tio 3d-elektroner. Observera också att g-orbitalerna är en rent teoretisk konstruktion eftersom ännu inga ämnen upptäckts som i grundtillståndet har elektroner i denna orbital. Man tror att sådana elektroner kan finnas bland ämnen med atomnummer från 121 eller 122 och uppåt.
Ytterligare ett exempel. Elektronkonfigurationen för silver är följande:
1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s1
vilket utläses som: 2 elektroner i 1s, 2 elektroner i 2s, 6 elektroner i 2p och så vidare.
Antal valenselektroner, det vill säga antalet elektroner i, och typen för, det yttersta skalet (det med högst energinivåer) är avgörande för ämnets kemiska egenskaper. Allt efter typen av detta skal brukar man också dela in det periodiska systemet i block: s-blocket, p-blocket, d-blocket och så vidare.
Se även
[redigera | redigera wikitext]Externa länkar
[redigera | redigera wikitext]Elementarladdning
[redigera | redigera wikitext]Elementarladdning, den minsta elektriska laddning som antas förekomma fritt i naturen, 1,602 177·10-19 coulomb.[1] Den elektriska laddningen hos en elektron, betecknas e-. Denna laddning ansågs länge vara den minsta möjliga laddning en partikel kan ha. I kvarkmodellen tillskrivs dock varje kvark en laddning som är antingen 1/3 eller 2/3 av elektronens laddning. Exempelvis består protonen av två kvarkar med laddning +2/3 och en med laddning -1/3, varvid protonladdningen blir lika stor som elektronens, men med motsatt tecken.
Elementarladdningens storlek bestämdes första gången med noggrannhet 1909 genom Millikans oljedroppsförsök.
Noter
[redigera | redigera wikitext]- ^ NIST (5 december 2007). ”Elementary charge”. 2006 CODATA recommended values. http://physics.nist.gov/cgi-bin/cuu/Value?e.
Elementarpartikel
[redigera | redigera wikitext]
Elementarpartiklar är materiens minsta beståndsdelar. Till elementarpartiklarna räknar man också de partiklar som är bärare av de fyra fundamentala krafterna i naturen. Elementarpartiklar studeras inom partikelfysiken, där de partiklar man för närvarande känner till beskrivs av den så kallade Standardmodellen.
Till elementarpartiklarna räknas
- kvarkarna
- leptonerna, exempelvis elektroner och neutriner
- fotonen, W-bosonerna, Z-bosonen och gluonen, samt de hypotetiska X-bosonerna, higgsbosonerna och gravitonerna.
Övriga partiklar är hadroner, som byggs upp av kvarkar. Hadronerna delas in i:
- baryoner som består av tre kvarkar – protoner och neutroner är exempel på baryoner –, och
- mesoner som består av två kvarkar (mer precist en kvark och en antikvark). Pi-mesoner är exempel på mesoner.
Hadroner är inte elementarpartiklar eftersom de är sammansatta av kvarkar.
Ett annat sätt att dela in elementarpartiklar är indelningen i fermioner och bosoner. Fermioner är de partiklar som materien är uppbyggd av, det vill säga kvarkar och leptoner, medan bosoner är bärarna av de fundamentala krafterna. De fundamentala fermionerna har spinn 1/2 och lyder under Fermi-Dirac-statistik, medan de fundamentala bosonerna har spinn 0 eller 1 och lyder under Bose-Einstein-statistik. Bland hadronerna är baryonerna fermioner och mesonerna bosoner.
Standardmodellen
[redigera | redigera wikitext]Standardmodellen är en kombination av två kvantfältteorier som beskriver alla nu kända partiklar och krafter. Den ena är den elektrosvaga växelverkan som förenar den elektromagnetiska och den svaga växelverkan och beskriver hur kvarkar och leptoner växelverkar med fotoner och W- och Z-bosoner genom den elektrosvaga växelverkan. Att dessa två typer av växelverkan är förenade betyder att vid höga energier är den elektromagnetiska och den svaga kraften olika aspekter av samma kraft. Den andra är kvantkromodynamiken, som beskriver hur kvarkar växelverkar med gluoner genom den starka växelverkan.
Fermioner
[redigera | redigera wikitext]De 12 fundamentala fermionerna delas upp i tre generationer med fyra partiklar vardera. Sex av partiklarna är kvarkar och sex är leptoner. Leptonerna består av tre neutriner och tre partiklar med elektrisk laddning -1: elektronen och dess två kusiner myonen och tau-leptonen.
Första generationen
|
Andra generationen
|
Tredje generationen
|
Det finns också 12 fundamentala fermioniska antipartiklar motsvarande de 12 partiklarna ovan. Positronen e+ är antipartikel till elektronen och så vidare:
Första generationen
|
Andra generationen
|
Tredje generationen
|
Bosoner
[redigera | redigera wikitext]Enligt Standardmodellen växelverkar elementarpartiklar genom de fundamentala krafterna, som förmedlas av bosoner med spinn 1. Detta är de så kallade vektorbosonerna eller gaugebosonerna: fotonen, gluonen, W-bosonerna och Z-bosonen. Dessutom finns teoretiskt i Standardmodellen Higgsbosonen, en spinn-0 boson som är ansvarig för att ge de andra partiklarna massa.
Gluonen
[redigera | redigera wikitext]Gluoner är masslösa och förmedlar den starka växelverkan. De växelverkar med alla partiklar som bär så kallad färgladdning, dvs. kvarkarna och gluonerna själva. Det är tex gluonerna som håller samman kvarkarna i protonerna och neutronerna.
Elektrosvaga bosonerna
[redigera | redigera wikitext]De tre svaga bosonerna förmedlar den svaga kraften. Detta är de elektriskt laddade W-bosonerna W+ och W-, och den elektriskt neutrala Z-bosonen. Den neutrala och masslösa fotonen förmedlar den elektromagnetiska kraften.
Higgsbosonen
[redigera | redigera wikitext]Higgsbosonen är ansvarig för att ge massa till W- och Z-bosonerna genom spontant symmetribrott. Detta kallas Higgsmekanismen. Higgsbosonen ger även massa till kvarkarna och de laddade leptonerna genom sin växelverkan. Higgsbosonen är den enda partikel i Standardmodellen som inte observerats experimentellt.
Historia
[redigera | redigera wikitext]Vetenskapens utveckling har efter hand förändrad begreppets mening. Det första kända föreställningen att världen bestod av grundläggande elementära delar var grekernas föreställning att materien bestod av de fyra elementen: luft, eld, jord och vatten.
Från grekernas tid och Demokritos härstammar också begreppet atom vilket betyder odelbar och fick sin nuvarande betydelse av bland andra John Dalton på 1800-talet. Under början av 1900-talet upptäckte man att atomen hade en inre struktur bestående av protoner, neutroner och elektroner. Antalet kända atomslag har med tiden växt och är idag omkring 117, varav 82 har stabila isotoper.
Under senare delen av 1900-talet upptäcktes nya elementarpartiklar. Införandet av kvarkar som hadronernas beståndsdelar kulminerade i tillkomsten av Standardmodellen i början av 1970-talet. Medan protonen och neutronen togs bort från listan av elementarpartiklar under denna process finns elektronen för närvarande kvar.
Idag finns teorier om hur även kvarkar och leptoner och de olika fundamentala krafterna kan förenas i en "Grand unified theory", eller om man inkluderar gravitationen, en "Teori om allt".
Se även
[redigera | redigera wikitext]- axion
- aggregationstillstånd
- antimateria
- fundamentala krafter
- kvantfysik
- materialism
- mörk materia
- partikelfysik
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Excitation
[redigera | redigera wikitext]I fysik innebär excitation (av latin: excitare, egga, stimulera) att energi tillförs en atom så att en elektron "hoppar upp" till ett skal som innehåller mer energi. Energin tillförs genom att en elektron exempelvis absorberar en foton, eller krockar med en närliggande atom eller partikel.
Exciterade atomer är mycket instabila. Efter en bråkdel av en sekund hoppar elektronen tillbaka till sitt grundskal, varvid den extra energin avges i form av elektromagnetisk strålning (ljus). Beroende på atomslaget, hur mycket energi som tillförts och huruvida elektronen hoppar tillbaka till sitt grundtillstånd i ett enda, eller flera steg, så kommer olika våglängder att utsändas.
Denna princip används till exempel i olika former av lysrör, där en tunn gas exciteras på elektrisk väg. Beroende på vilka ämnen som finns i röret kan man få fram olika färger på det utsända ljuset. Det utstrålade ljuset har väldigt specifika våglängder, vilket gör att fenomenet kan användas för att beräkna vilka ämnen ett visst prov består av. Detta används i synnerhet inom astronomi för att bestämma vilka grundämnen olika stjärnor är uppbyggda av.
Se även
[redigera | redigera wikitext]Faradays lag
[redigera | redigera wikitext]Faradays induktionslag är en grundläggande lag inom elektromagnetismen, upptäckt av och namngiven efter Michael Faraday och formulerad av James Clerk Maxwell som är viktig för hur transformatorer, spolar och många andra sorters elektriska generatorer fungerar.
Lagen säger att i en sluten elektrisk ledare i ett tidsvarierande magnetfält induceras en elektromotorisk kraft, en elektrisk spänning, och att denna elektromotoriska kraft är lika med tidsderivatan av det magnetiska flödet. Förenklat kan man säga att ju snabbare magnetfältet förändras, desto högre spänning uppkommer i ledaren.
En generator är en konkret tillämpning av Faradays lag.
Härledning
[redigera | redigera wikitext]Från Maxwells ekvationer har vi:
Om vi definierar:
- =emf inducerad i kretsen med konturen C (Volt)
och
- =magnetiskt flöde genom ytan S (Weber)
så får vi att:
- (Volt)
Se även
[redigera | redigera wikitext]Källor
[redigera | redigera wikitext]- Cheng David K, Field and Wave Electromagnetics, Second Edition, Fourth Printing, 1991, USA & Canada
Fermi-Dirac statistik
[redigera | redigera wikitext]
Fermi-Dirac-statistiken bestämmer sannolikhetsfördelningen för fermioners (till exempel elektroner i fasta kroppar tillhörande valens- och ledningsbanden) energitillstånd som funktion av temperaturen. Sannolikheten n(ε) för att en fermion befinner sig i ett kvanttillstånd med energin ε vid temperaturen T kan tecknas
där
- är den aktuella energinivån
- är den kemiska potentialen
- är Boltzmanns konstant
- är temperaturen
Vid temperaturer nära absoluta nollpunkten är för varje energinivå sannolikheten nära 1 för att energinivån är besatt. Vid låga temperaturer () är lika med Ferminivån.
Se även
[redigera | redigera wikitext]Fermion
[redigera | redigera wikitext]En fermion är en partikel med halvtaligt spinn. Det är också en klass av elementarpartiklar med denna egenskap. Exempel på fermioner är elektronen, protonen, neutronen, neutrinon samt kvarkarna. Även atomer eller atomkärnor med halvtaligt spinn är fermioner.
Alla fermioner har alltså spinn vars värde är en udda multipel av 1/2, (d.v.s. 1/2, 3/2, 5/2, etc.) multiplicerat med Plancks konstant dividerad med 2π (d.v.s. ).
Fermioner lyder under Paulis uteslutningsprincip och Fermi-Dirac-statistiken.
Se även
[redigera | redigera wikitext]Galvanometer
[redigera | redigera wikitext]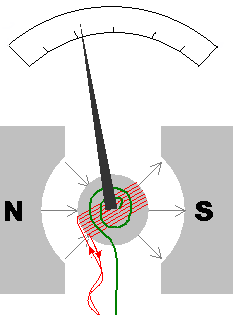
Ett vridspoleinstrument eller en galvanometer är en känslig elektromekanisk anordning för att mäta små elektriska strömmar. På 1900-talet var amperemetrar och voltmetrar oftast baserade på vridspoleinstrument, men nu används för de flesta tillämpningar elektroniska multimetrar.
Katodstrålerör
[redigera | redigera wikitext]
1. Elektronkanoner (3 stycken)
2. Elektronstrålar (3 stycken)
3. Fokuserings-spolar
4. Avlänkningsspole
5. Anodens anslutning
6. Nät/mask för att separera de tre strålarna
7. FosforlageFet textr på bildskärmsytan
8. Närbild på insidan av skärmen med separeringsmasken och fosfor-ytan som är indelad i fält för de tre färgerna
Katodstrålerör, benämns ofta CRT (eng. Cathode Ray Tube) när det används om datorskärmar, är den skärmteknik som under lång tid var standard för datorskärmar, övervakningsskärmar, TV-apparater Spektrumanalysator och oscilloskop, i dag nästan helt ersatt av LCD- och plasmateknik. Katodstråleröret uppfanns av Ferdinand Braun och namnet kommer ifrån katodstråle.
Katodstrålar är strömmar av elektroner i hög hastighet som emitteras av den uppvärmda katoden i röret som är lufttomt. Elektronerna accelereras därefter i ett elektriskt fält upp till en erforderlig rörelseenergi varefter elektronstrålen avlänkas (styrs och ändrar riktning) med hjälp av elektriska eller magnetiska fält. Efter positioneringen färdas elektronerna vidare innan de träffar en fluorescerande yta (anod). När elektronerna krockar med denna ytas atomer emitteras ljus.
Avlänkning (ty. Ablenkung, eng. deflection) med elektriska fält användes i oscilloskop, eftersom avlänkningen är oberoende av frekvensen hos de avböjande signalerna, vilket är viktigt i ett mätinstrument. Fältet skapas av platta elektroder inne i röret. Nackdelen är att bildröret blir långt och apparaten djup, samtidigt som bildskärmens yta blir förhållandevis liten. I TV-mottagare och datorskärmar, där stor bildyta och kort inbyggnadsdjup är viktigt, användes i stället avlänkning med magnetfält genom avlänkningsspolar (eng. deflection coil) utanpå bildröret. Avböjningen sker i dessa fall med fasta frekvenser, ex.vis 50 Hz i vertikalled och 15625 Hz i horisontalled för CCIR/PAL TV.
CRT-skärmens fördelar
[redigera | redigera wikitext]- Billigare än LCD- och Plasmaskärmar
- Bra färgåtergivning och kontrast
CRT-skärmens nackdelar
[redigera | redigera wikitext]- Tillverkas inte i storlekar över 36" tum
- Ljusstyrkan försämras med tiden något fortare än LCD
- Tung, upp mot 50-60 kg
- Tillverkas inte längre (Datorskärmar och TV-apparater)
Tillverkare som upphört med sin CRT-skärmstillverkning
[redigera | redigera wikitext]- Dell
- Fujitsu
- Hitachi
- LG Electronics
- Luxor
- Mark
- NEC
- Nokia
- Panasonic Corporation (tidigare Matsushita)
- Philips
- Pioneer
- Samsung
- Sony
- Toshiba
Se även
[redigera | redigera wikitext]Teknik för bildskärmar
[redigera | redigera wikitext]Övrigt
[redigera | redigera wikitext]Kvantelektrodynamik
[redigera | redigera wikitext]Kvantelektrodynamik (QED efter engelska Quantum electrodynamics) är en fysikalisk teori grundad på kvantfysik och elektrodynamik som kan sägas vara en tillämpning av kvantfältteori på elektromagnetiska fält. Teorin utvecklades av bland annat Richard Feynman, Shinichiro Tomonaga och Julian Schwinger. Dessa tre fick för detta nobelpriset i fysik 1965.
Under 1940-talet hade Feynman, Schwinger och Tomonaga var för sig lyckats visa att elektromagnetismen kunde skrivas som en fullgod kvantteori. Problemet var att enligt den relativistiska kvantmekaniken kan partiklar skapas om man har tillräckligt med energi. Detta betyder att då man sprider en elektron mot en annan elektron kan man skapa t ex ett extra elektron-positronpar. Har man inte tillräckligt med energi kan man ändå skapa dem virtuellt, eftersom Heisenbergs osäkerhetsprincip säger att så länge detta par lever tillräcklig kort tid kan det skapas. Detta betyder att man måste behandla teorin som en mångpartikelteori, en kvantfältteori, där man kan skapa ett godtyckligt antal partiklar så länge detta inte strider mot osäkerhetsprincipen.
Feynman beskrev detta med sina berömda Feynmandiagram. Varje process kan i en störningsutveckling skrivas som en oändlig serie av allt mer komplicerade diagram. I den N:e ordningen finns det ungefär N! olika diagram. Alla diagram utom den lägsta ordningen beskrivs av oändliga integraler som måste renormeras, dvs göras ändliga, för att man skall få någon mening i teorin. Vad de tre ovan visade var att alla dessa oändligheter kunde klassificeras i tre klasser och genom att låta elektronmassan, elektronladdningen och vågfunktionens normering vara obestämda kunde alla diagram renormeras.
De tre storheterna kunde sedan bestämmas experimentellt. Detta var en stor vetenskaplig framgång som gjorde att teori kunde jämföras med experiment med upp till elva decimalers noggrannhet. Man trodde så på 1950-talet att det skulle vara en öppen väg att också finna kvantfältteorier som beskrev de andra fundamentala växelverkningarna. Detta stötte dock omgående på patrull. För den starka kärnkraften förslog man en teori som verkligen var renormerbar men utvecklingsparametern, som måste vara liten för att de skall fungera, visade sig vara större än ett.
Lepton
[redigera | redigera wikitext]
Leptoner är elementarpartiklar enligt kvantfysiken.
Leptonerna är den ena huvudgruppen av fermioniska elementarpartiklar. Den andra gruppen är kvarkarna. Av leptoner finns det sex stycken aromer, vilka liksom kvarkarna delas in i tre familjer. Varje familj består av en partikel och tillhörande neutrino.
- familj 1: elektron, elektronneutrino
- familj 2: myon, myonneutrino
- familj 3: tau-lepton, tauneutrino
Neutrinerna har ingen laddning medan de övriga leptonerna har laddningen -e (elementarladdningen).
| Namn | Symbol | Laddning | Massa (MeV/c2) |
|---|---|---|---|
| Elektron | e- | -e | 0,511 |
| Elektronneutrino | νe | 0 | < 3 eV |
| Myon | μ- | -e | 105,6 |
| Myonneutrino | νμ | 0 | < 0,19 |
| Tauon | τ- | -e | 1777 |
| Tauneutrino | ντ | 0 | < 18,2 |
Alla dessa sex aromer har också varsin antipartikel med motsatt laddning. Elektronens antipartikel har ett eget namn, positron (e+).
Skillnaden mellan leptoner och kvarkar
[redigera | redigera wikitext]Den viktiga skillnaden mellan leptoner och kvarkar är att leptoner växelverkar svagt medan kvarkar växelverkar både svagt och starkt.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Magnetisk dipol
[redigera | redigera wikitext]Magnetisk dipol, ett objekt som har ett magnetiskt dipolmoment. Eftersom en magnetisk monopol inte är känd, är magnetisk dipol en annan term för magnet.
Många elementarpartiklar med spinn har ett magnetiskt dipolmoment: elektron, myon, osv. Protonens och neutronens magnetiska moment är mycket mindre, men många atomkärnors magnetiska dipolmoment kan studeras med kärnmagnetisk resonans.
Enheter och storheter
[redigera | redigera wikitext]Även en elektrisk ström genom en ringformig ledare är en magnetisk dipol. På avstånd som är mycket större än ringens radie, har fältet formen av ett dipolfält. Dipolens styrka (dipolmoment) är μ =I·A där I är strömmen och A är cirkelns area. En typisk storleksordning av atomära moment är bohrmagnetonen. Dipolmomentet har i SI-systemet enheter A·m² som är lika med J/T. Enheten Am² visar sambandet med magnetisering som dipolmoment per volymenhet.
I ett homogent magnetfält är den totala kraften på en dipol lika med noll, och det kan bara finnas ett vridmoment som ges av:
där B är det magnetiska B-fältet (flödestäthet). Vridmomentet är noll när momentet är parallellt med fältets riktning. I detta läge är energin minimal, och man kan skriva:
där φ är vinkeln mellan magnetfältet och dipolens riktning. Skillnaden i energi mellan parallellt och antiparallellt läge är därför:
Exempel
[redigera | redigera wikitext]Atomer med oparade elektroner kan ha stora magnetiska moment. Exempel är gadolinium-atomen med 7 parallella elektronspinns i 4f-orbitalerna och Fe3+ med 5 parallella elektroner i 3d-orbitalerna. Även syre-molekylen med dess två oparade elektroner är en liten magnet, något som ger upphov till paramagnetism.
Ferromagnetism kan uppstå när det finns växelverkningar som gynnar en parallell orientation av grannatomers magnetiska moment, till exempel i gadolinium under dess Curie-temperatur på 280 K.
Se även: Elektrisk dipol.
Metall
[redigera | redigera wikitext]Metall kallas ett grundämne eller en legering med metalliska egenskaper, till exempel hög ledningsförmåga för elektricitet och för värme, formbarhet, i allmänhet hög densitet och metallglans. Några viktiga och välkända metaller är aluminium, bly, guld, järn, koppar, platina, silver, tenn och zink. Metall har haft stor betydelse i människans historia, vilket återspeglas i namn på epoker som bronsåldern och järnåldern.
Metaller inom kemin
[redigera | redigera wikitext]Metaller är den största gruppen av grundämnen, omkring 80% av alla grundämnen är metaller. I det periodiska systemet är metallerna inte inordnade i raka grupper eller perioder utan återfinns under och till vänster om en diagonal linje från bor till polonium vilka kallas halvmetaller. Över och till höger om samma linje finns icke-metallerna.
Traditionellt delar man in metallerna efter densiteten i lättmetaller och tungmetaller, och efter dess påverkan av omgivningen i ädla och oädla metaller. I nedanstående tabell visas en översikt över metallernas indelning i det periodiska systemet vad gäller densitet.
| H | He | |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Li | Be | B | C | N | O | F | Ne | |||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |
| Cs | Ba | La | * | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| Fr | Ra | Ac | ** | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | |||||||
| * | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | ||||
| ** | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | ||||
| Lättmetaller < 5 g/cm³ | Tungmetaller < 10 g/cm³ | Tungmetaller > 10 g/cm³ |
Egenskaper
[redigera | redigera wikitext]Metallatomer känns igen på följande kemiska egenskaper:
- antalet elektroner i det yttre skalet är litet och mindre än koordinationstalet.
- joniseringsenergin är liten, mindre än ungefär 10 eV.
Detta innebär att metallatomerna lätt släpper ifrån sig valenselektroner och bildar positivt laddade joner (katjoner), som hålls samman av metallbindningar och bildar ett metallgitter, en kristallin struktur. Gittret ger metallen dess formbarhet och de fria elektronerna som finns i ett gemensamt "elektronmoln" gör att metaller är utmärkta värme- och elektriska ledare, samt gör att metallen blir reflektiv. Det gör också att ämnet absorberar åtskilliga ljusvåglängder vilket resulterar i att metaller har en grå, silvrig till svart färg och är ogenomskinliga. Den relativt starka metallbindningen gör att metaller i allmänhet har en hög smältpunkt.
Metaller är i allmänhet instabila ämnen, dess yta reagerar ofta med till exempel den omgivande luften och korroderar. Järn rostar sönder under flera år och kalium brinner upp på ett par sekunder. För att förhindra korrosionen kan man behandla metallen på olika sätt, till exempel genom att täcka ytan med färg eller genom anodisering.
Legeringar
[redigera | redigera wikitext]Legeringar är material med metalliska egenskaper vilket består av två eller flera grundämnen (legeringskomponenter), varav minst ett är metall. Några kända legeringar är amalgam, brons, mässing och stål.
Ädelmetaller
[redigera | redigera wikitext]En ädelmetall är ett metalliskt grundämne med högt ekonomisk värde. Hit brukar räknas guld, silver och platina. Ädelmetaller bildar inte gärna joner. Inom kemin räknas även koppar som ädelmetall.
Se även
[redigera | redigera wikitext]Molekyl
[redigera | redigera wikitext]
En molekyl definieras som en grupp av två eller fler atomer ordnade i ett precist arrangemang med hjälp av kovalenta bindningar.[1][2][3]
En molekyl kan variera i storlek från två atomer, till exempel H2 (vätgas), till tusentals atomer i makromolekyler som proteiner, nukleinsyror eller syntetiska och naturliga polymerer. Det kan också förekomma jonbindningar, vätebindningar och andra typer av kemiska bindningar mellan olika delar av molekylen, men det är bara kovalenta bindningar som alltid är mellan atomer i samma molekyl.
Inom den kinetiska gasteorin används ofta termen molekyl för alla partiklar i gasform oavsett dess beståndsdelar. Enligt denna definition räknas ädelgaser som molekyler trots att de endast består av enkla obundna atomer.[4] Proteiner med kvartärstruktur består i själva verket i många fall av flera molekyler som hålls samman av intermolekylära krafter, även om biokemister ofta betraktar dem som en enda molekyl.
Laddning
[redigera | redigera wikitext]När man talar om små molekyler antas de normalt vara oladdade. Kovalent bundna atomgrupper som är laddade kallas i stället sammansatta joner. För större molekyler, särskilt biokemiska makromolekyler, är terminologin mindre precis, så sådana molekyler kan ha en nettoladdning som inte är noll. Naturligt laddade molekyler och molekyler som har gjorts laddade kan separeras med tekniker som elektrofores och masspektrometri.
Polaritet
[redigera | redigera wikitext]
Om molekylens atomer har olika elektronegativitet kommer den kovalenta bindningen att bli polariserad. Om polärt kovalenta bindningar är ojämnt fördelade över molekylen får den en positivt och en negativt laddad sida – den blir en dipol. Ett exempel är vattenmolekylen – syre och väte har olika elektronegativitet, och eftersom vattenmolekylen dessutom är böjd blir den en dipol. Koldioxid är däremot inte en dipol eftersom de båda bindningarna ligger i linje med varandra.
Molekylärvetenskap
[redigera | redigera wikitext]Molekyler studeras i många vetenskapsfält som med ett samlingsnamn kallas molekylärvetenskap. De omfattar, förutom i stort sett alla grenar av kemin, även bland annat molekylfysik, kemisk fysik och molekylärbiologi. Avstånden mellan atomer i molekyler mäts typisk i enheten ångström, alltså 10-10 meter. I den storleksskalan är kvantmekaniken den fysikaliska teori som bäst beskriver hur materien uppför sig. Den elektromagnestiska strålning som har en våglängd i mätt i ångström kallas för röntgenstrålning och kan användas för att studera formen på molekyler i kristallin form genom röntgendiffraktion. För studiet av molekyler i lösning är kärnmagnetisk resonansspektroskopi en användbar metod. Nu är dock inte formen på molekyler det enda intressanta fenomen som går att studera.
Med hjälp av spektroskopiska metoder går det att klura ut många av molekylernas inre strukturer. Molekyler är inte stilla. De rör sig i rummet, vibrerar och roterar. Dessutom kan elektronerna i molekylerna anta olika energinivåer beroende på vilken molekylorbital de ockuperar. Beroende på vad som studeras kan olika modeller användas. Energin är kvantiserad och molekyler som byter energitillstånd kan ta, upp, sända ut, och växelverka med fotoner.
Molekyler kan också reagera med varandra och bilda nya molekyler. Den organiska kemin studerar främst kolbaserade molekyler medan den oorganiska kemin studerar andra typer av molekyler. Biokemin studerar molekyler och dess reaktioner i biologiska system. Med hjälp av termodynamiken går det att säga om en reaktion kommer att ske spontant och vid vilka koncentrationer kemisk jämvikt uppkommer.
Beskrivning av molekyler
[redigera | redigera wikitext]En empirisk formel beskriver andelen atomer av olika sorter i förhållande till varandra i en molekyl. En summaformel anger hur många atomer av varje atomslag som finns i en molekyl. Eftersom olika molekyler kan ha både samma empiriska formel och samma summaformel så har det utvecklats olika standarder för strukturformler. Molekyler som har samma summaformel men olika strukturformel sägs vara isomerer. VSEPR-teorin är en teoretisk och förhållandesvis enkel modell för att förutsäga vilken form en molekyl har utifrån dess strukturformel. Delar av den analytiska kemin ägnar sig åt att empiriskt bestämma strukturen på molekyler. Beräkningskemister använder datorer för att utifrån kvantmekaniken teoretiskt beräkna olika egenskaper hos molekyler.
Referenser
[redigera | redigera wikitext]- Den här artikeln är helt eller delvis baserad på material från engelskspråkiga Wikipedia, Molecule, tidigare version.
- ^ ”Molecule” (på engelska). IUPAC Gold Book. 1994. http://goldbook.iupac.org/M04002.html. Läst 9 november 2010.
- ^ Ebbin, Darrell, D. (1990) (på engelska). General Chemistry (3:e upplagan). Boston: Houghton Mifflin Co. ISBN 0-395-43302-9
- ^ Brown, T.L. (2003) (på engelska). Chemistry – the Central Science (9:e upplagan). New Jersey: Prentice Hall. ISBN 0-13-066997-0
- ^ Chandra Sulekh. Comprehensive Inorganic Chemistry. New Age Publishers. ISBN 8122415121 språk=engelska. http://books.google.se/books?id=TQhN9_5y7VAC&printsec=frontcover&dq=ISBN%3D8122415121&source=bl&ots=4sZ9GIdtjZ&sig=uD6s3ehimBOKqxdu5QYRfRaGn-E&hl=sv&ei=i4zZTPLMKYqfOuWpiOYI&sa=X&oi=book_result&ct=result&resnum=1&ved=0CBwQ6AEwAA#v=onepage&q&f=false
Positron
[redigera | redigera wikitext]En positron är elektronens antipartikel. Den har samma massa och har en lika stor men motsatt laddning som elektronen. Positronens laddning är +1 och har ett spinn på 1/2.
När en positron och en elektron kolliderar annihileras (förintas) båda och resulterar i två gammafotoner. Detta sker dock långtifrån ögonblickligen. I normalfallet bromsas positronen upp tills dess den har omkring samma rörelseenergi som elektronerna i materialet, varpå den bildar en så kallad positroniumatom tillsammans med en vanlig elektron (och joniserar därmed den atom som elektronen kom ifrån). En sådan "atom" existerar sedan i storleksordningen 0,1 nanosekunder innan den slutligen annihileras.
Positroner kan uppkomma genom positronutsläpp (betasönderfall) från radioaktiva material eller vid parproduktion från en energifylld foton.
Diracekvationen, som utarbetades av Paul Dirac 1928 och är en generalisering av Schrödingerekvationen inom kvantmekaniken som även tar hänsyn till den speciella relativitetsteorin, postulerade existensen av positroner fyra år före det att partikeln 1932 upptäcktes av Carl D. Anderson. Det var första gången som en elementarpartikel först förutsagts teoretiskt innan den upptäckts experimentellt, något som blivit relativt vanligt sedan dess.
Statisk elektricitet
[redigera | redigera wikitext]
Statisk elektricitet är elektriska laddningar och fält i vila.
Fenomenet statisk elektricitet uppkommer efter att två föremåls ytor åtskiljs, efter att ha varit i kontakt med varandra. Anledningen är att elektronerna dras med olika kraft till olika material. Uppladdningen blir större när två föremål gnids mot varandra, därför att kontaktytan då ökar.
Ett klassiskt exempel på statisk elektricitet är den som bildas vid kamning av torrt, nytvättat hår. Då fastnar det negativt laddade elektroner på kammen, vilket ger upphov till en laddning i både kammen och håret.
Statisk elektricitet är farlig för många elektronikkomponenter, såsom minnen och IC-kretsar. I vissa branscher där man till exempel hanterar drivmedel och sprängämnen är statisk elektricitet ett kritiskt säkerhetsproblem.
Statiska laddningar kan bli ett stort problem vid tillverkning av exempelvis plastprodukter, som plastpåsar, laddade påsar fastnar vid varandra. Problemen kan också vara stora på tryckerier, ark som blir laddade fastnar lätt överallt.
Inom industrin används avjoniserings-utrustningar och avelektrifierings-utrustningar som motverkar och avleder den statiska elektriciteten / laddningarna.
Se även
[redigera | redigera wikitext]Externa länkar
[redigera | redigera wikitext]![]() Wikimedia Commons har media som rör Knoppson/Elektroteknik.
Wikimedia Commons har media som rör Knoppson/Elektroteknik.
Subatomär partikel
[redigera | redigera wikitext]Subatomära partiklar är ett samlingsbegrepp för fysikaliska partiklar som är mindre än atomer. Dessa kan vara elementära eller sammansatta, och studeras tillsammans med hur de agerar inom partikel- och kärnfysik.
I begreppet ingår bland annat de tre partikeltyper som bygger upp atomer: elektroner, protoner och neutroner, där de två senare i sin tur består av de likaledes i begreppet ingående kvarkarna.
Alfapartikeln, deuteronen och de andra nukliderna är också subatomära. Dessutom ingår fotoner och neutriner, där de senare uppstår i radioaktiva processer i bland annat solen, samt ett flertal typer som inte kan observeras under normala energiförhållanden på jorden, men som ingår i kosmisk strålning och kan produceras i partikelacceleratorer.
Beroende på partiklarnas spinn delas de in i bosoner och fermioner.
Thomsonspridning
[redigera | redigera wikitext]Thomsonspridning är spridning av elektromagnetisk strålning mot en fri laddad partikel i vila, särskilt mot fria elektroner. Spridningsmekanismen är uppkallad efter J.J. Thomson och gäller bara för fotonenergier mycket mindre än elektronens vilomassa. Vid Thomsonspridning har den inkommande vågen samma frekvens som den utgående vågen. Därför kallas denna spridning även koherent eller elastisk. Träffytan för denna spridningsmekanism ges av elektronens klassiska radie.
Om fotonens energi är större eller även elektronen rör på sig, blir processen mer komplicerad och kallas Comptonspridning. Om elektronen är bunden i atomer talar man om Rayleighspridning.
Klassisk icke-relativistisk behandling
[redigera | redigera wikitext]En fri laddning accelereras av det oscillerande elektriska fältet E av en plan inkommande våg, fram och tillbaka med samma frekvens som strålningsfältet. Det ger upphov till en sfärisk våg, med utstråld effekt per rymdvinkel i riktningar med spridningsvinkel θ:
där <a ²> anger ett tidsmedelvärde äver accelerationen a=qE/m.
Genom att normalisera med energiflödet av det inkommande fältet kan man definiera en differentiell träffyta:
där re = 2,818.10-15 meter är den klassiska elektronradien.[1]
Den totala thomsonträffytan för en elektron är
Atomer
[redigera | redigera wikitext]När det inkommande strålningsfältet har en fotonenergi som är mycket större än bindningsenergin, kan även bundna elektroner betraktas som fria. Så är till exempel fallet för lätta atomer i röntgenområdet. När våglångden är stor i förhållande till atomen, oscillerar elektronerna i det oscillerande fältet i fas med varandra, så att deras strålning adderas koherent. Atomens koherenta träffyta är därför ungefär lika med kvadratet av antalet elektroner gånger thomsonträffytan.
För strålning med en fotonenergi som är mycket lägre än bindningsenergi, är träffytan mycket mindre och starkt frekvensberoende, se Rayleighspridning. Nära resonanser kan atomära spridningsfaktorer vara mycket stora.
Källor
[redigera | redigera wikitext]- Richard Fitzpatrick (2006). ”Thomson scattering”. Classical Electromagnetism : An intermediate level course. http://farside.ph.utexas.edu/teaching/em/lectures/node96.html.
Fotnoter
[redigera | redigera wikitext]- ^ ”Classical electron radius”. 2006 CODATA recommended values. NIST. http://physics.nist.gov/cgi-bin/cuu/Value?re.
- ^ ”Thomson cross section”. 2006 CODATA recommended values. NIST. http://physics.nist.gov/cgi-bin/cuu/Value?sigmae.
Valenselektron
[redigera | redigera wikitext]En valenselektron är en elektron i atomens yttersta skal (valensskalet). Antalet valenselektroner har stor betydelse för vilka kemiska föreningar atomen kan ingå i, det vill säga antalet bestämmer atomslagets kemiska egenskaper. Se periodiska systemet. Syre har 6 och klor har 7 valenselektroner.
Huvudvalensbindningar är bindningar mellan atomer i en molekyl och bivalensbindningar är bindningar mellan olika molekyler. Huvudvalensbindningarna är kovalenta bindningar. Dessa är starka och kan endast brytas genom kemiska reaktioner. Bivalensbindningarna är också av elektrisk natur och orsakas av van der Waals-krafter. Bivalensbindningarna är svaga.
Zeemaneffekt
[redigera | redigera wikitext]Zeemaneffekten är en magnetooptisk effekt, där en delning av en spektrallinje uppstår i ett magnetfält. Den har fått sitt namn efter Pieter Zeeman, som 1896 beskrev fenomenet för första gången.[1]
Motsvarande effekt av ett elektriskt fält kallas Starkeffekten.
Referenser
[redigera | redigera wikitext]- ^ Pieter Zeeman (1897). ”The Effect of Magnetisation on the Nature of Light Emitted by a Substance”. Nature 55: sid. 346. http://www.nature.com/physics/looking-back/zeeman/index.html.
Se även
[redigera | redigera wikitext]Laddning (Q)
[redigera | redigera wikitext]Vetenskapen har svårt för att definiera exakt vad en laddning är för något men helt klart är att den dels har tecken (lika laddningar repellerar, olika attraherar) dels kan kvantiseras som en Coulomb (C) eller As efter elektronens laddning (1.602*10-19 C). Kraften mellan två laddningar är sedan:
Originalartikel
[redigera | redigera wikitext]

Elektrisk laddning eller elmängd[1] (Q, q) är den fysikaliska storhet som påverkas av elektromagnetisk växelverkan, en av de fyra fundamentala krafterna.
I Coulombs lag har laddning samma roll som massa i Newtons gravitationslag, men skillnaden är att laddning kommer i två varianter, positiv och negativ. Det finns också en fundamental skillnad med de tre typer av färgladdning i den starka växelverkan.
Att det finns två och endast två typer av statisk elektricitet har varit känt sedan 1700-talet. Du Fay myntade termerna vitreös och resinös, för "glaselektricitet" och "hartselektricitet".[2] Laddningar av samma typ repellerar varandra, medan växelverkan mellan laddningar av olika typ är attraktiv. Benjamin Franklin upptäckte att man kunde betrakta dessa som positiva och negativa laddingar, vars algebraiska summa är konserverad. Detta betyder att den totala laddning varken kan förnyas eller förintas, vilket gör den till en av de elementära egenskaper materia besitter.
Elektrisk laddning är kvantiserad till negativa eller positiva multipler av elementarladdningen e. Kvarkars laddninger är ±⅓e eller ±⅔e, men de förekommer inte fria.
Enheter och mätning
[redigera | redigera wikitext]Inom SI betecknar elektricitetsmängden en mängd elementarladdningar, där laddningsenheten är |e| = 1,602 177 33·10-19 coulomb (vanligtvis är e den positiva laddningen för protonen, medan -e är den negativa laddningen för elektronen).
Elektricitetsmängd kan mätas med elektrometer. Det har enheten coulomb. Formern för beräkning är I = Q/t, Före upptäckten av Robert A Millikans elektron, som genomfördes genom att fallande oljedroppar observerades, brukades termerna anjon (jon betyder "strövare") och katjon användas, introducerade av Michael Faraday.
En (1) elektricitetsmängd kan definieras som den mängd laddningar som passerar genom en tvärsnittsyta i en elektrisk ledare under en ström på en (1) ampere under en (1) sekund. Formellt bör en sådan kvantitet vara en multipel av elementärladdningen e, men eftersom det är ett medelvärde kan det vara vilket reellt tal som helst.
Noter
[redigera | redigera wikitext]- ^ Svenska Elektriska Kommissionen (1988). ”Elektricitet och magnetism (1971)”. SI måttenheter: Storheter och enheter. Stockholm: Swedish Standards Institute
- ^ Charles François de Cisternay du Fay (5 december 1734). ”A Discourse concerning Electricity”. Philosophical Transactions. http://www.sparkmuseum.com/BOOK_DUFAY.HTM.
Ström (I)
[redigera | redigera wikitext]Ström är laddningar i rörelse enligt
där q kan vara positivt för hål (halvledare) och negativt för elektroner. n är laddningstätheten och v är hastigheten laddningarna rör sig med. Enheten för ström är Ampere (A).
Spänning (U)
[redigera | redigera wikitext]Spänning är detsamma som potentialskillnad. Om det flyter samma ström genom två olika motstånd kommer det största motståndet ha störst potential och därmed spänning. Enheten är Volt (V). Otroligt korkad definition...
Resistans (R)
[redigera | redigera wikitext]Resistans är ett mobilitetsfenomen. Det definieras som (tråd):
där är resistiviteten hos det ledande mediumet, l längden och A tvärsnittsarean.
Resistans är det motstånd strömmen möter när det flyter genom en komponent. Enheten är Ohm ().
Effekt (P)
[redigera | redigera wikitext]Effekt är produkten av ström och spänning. Det kan liknas vid ett slags arbete (jfr bil och hp). Det är ofta en så kallad förlusteffekt man avser men även nyttiga effekter såsom i slutsteg av olika slag. Enheten är Watt (W).
Ohm's lag
[redigera | redigera wikitext]Ohm's lag säger att
där
och
.
Elektrisk potential (V)
[redigera | redigera wikitext]En elektrisk potential satisfierar i dom flesta fall Poissons ekvation
vilket alltså innebär att den volymsmässiga förändringens förändring av potentialen är lika med -.
I det här fallet står alltså för laddninstätheten och Poissons ekvation kan härledas ur Maxwells ekvationer nedan.
Elektrisk fältstyrka (E)
[redigera | redigera wikitext]Elektrisk fältstyrka definieras som derivatan av potentialen map sträckan eller
Enheten är V/m.
Elektriskt förskjutningsfält (D)
[redigera | redigera wikitext]Elektriskt förskjutningsfält definieras som
där är permitiviteten, dvs den elektriska laddningsförmågan, hos mediumet.
Kanske...
Magnetisk fältstyrka (H)
[redigera | redigera wikitext]Magnetisk fältstyrka definieras som derivatan av strömmen map sträckan eller
Enheten är A/m.
Säkert :-)
Magnetisk flödestäthet (B)
[redigera | redigera wikitext]Magnetisk flödestäthet definieras som
där är permeabiliteten, dvs den magnetiska ledningsförmågan, hos mediumet. Enheten är Tesla (T).
Magnetiskt flöde ()
[redigera | redigera wikitext]Magnetiskt flöde definieras som
där S står för yta (Surface). Enheten är Wb (Weber).
Strömtäthet (J)
[redigera | redigera wikitext]Strömtäthet är strömmen genom en ledare delat med arean eller
Enheten är A/m2.
Maxwells ekvationer
[redigera | redigera wikitext]Maxwells ekvationer innehåller allt som dagens teknik och telekommunikation bygger på. Ett par exempel är vågledare och antenner. De är till antalet endast fyra och visas här på integralform.
Läs mer på Maxwells ekvationer
Kapacitans (C)
[redigera | redigera wikitext]Kapacitans är ett dielektriskt fenomen. Definitionen av kapacitans är:
där enheten är C/V eller As/V eller Farad (F). I praktiska fall leder detta till:
som formel för två plattor i ett (isolerande) dielektriskt medium definierat av permitiviteten , arean A hos plattorna samt d avståndet mellan plattorna. Enheten är Farad.
Induktans (L)
[redigera | redigera wikitext]Induktans är ett magnetiskt fenomen. Definitionen av induktans är:
där enheten är Wb/A eller Vs/A eller Henry (H). I praktiska fall leder detta till:
som formel för en rak spole i ett magnetiskt medium definierat av permeabiliteten , tvärsnittsarean A, antal varv N samt den magnetiska längden lm. Enheten är Henry (H).
Reaktans
[redigera | redigera wikitext]Reaktans kallas det sinusiala motståndet hos en reaktiv komponent (L eller C). Enheten är Ohm ().
En kondensators reaktans (XC)
[redigera | redigera wikitext]Strömmen genom en kondensator definieras av:
dvs den beror på hur pass snabbt spänningen varierar map tiden. I sinusiala eller så kallade stationära fall kan man skriva denna formel med hjälp av jw-metoden som:
Ur denna formel kan man sedan få att:
vilket är beteckningen för en kondensators så kallade reaktans eller sinusiala motstånd för strömmen. jw kommer f.ö från den så kallade Fourieranalysen och betyder (tonvis) derivering.
En spoles reaktans (XL)
[redigera | redigera wikitext]Spänningen över en induktans (vilket är detsamma som spole) definieras av:
dvs den beror på hur pass snabbt strömmen ändrar sig map tiden. I sinusiala eller så kallade stationära fall kan man skriva denna formel med hjälp av jw-metoden som:
Ur denna formel kan man sedan få att:
vilket är beteckningen för en spoles så kallade reaktans eller sinusiala motstånd för strömmen. jw kommer f.ö från den så kallade Fourieranalysen och betyder (tonvis) derivering. Det är även intressant att notera teckenskillnaden. I jämförelse med en kondensator kommer alltså strömmen vara 180 grader ur fas.