Νησίδια του Λάνγκερχανς
| Νησίδια του Λάνγκερχανς | |
|---|---|
 Τα παγκρεατικά νησίδια είναι ομάδες κυττάρων απαντώμενων μέσα στο πάγκρεας και εκκρίνουν ορμόνες | |
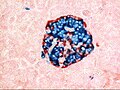
 Παγκρεατικό νησίδιο ποντικού σες τυπική θέση, πλησίον αιμοφόρου αγγείου. Η ινσουλίνη εμφανίζεται με κόκκινο χρώμα, οι πυρήνες με μπλε. | |
| Λεπτομέρειες | |
| Μέρος του | Πάγκρεας |
| Σύστημα | Ενδοκρινικό σύστημα |
| Αναγνωριστικά | |
| Λατινικά | insulae pancreaticae |
| MeSH | D007515 |
| TA | A05.9.01.019 |
| FMA | 16016 |
| Ορολογία ανατομίας | |
Τα παγκρεατικά νησίδια (ή νησίδες) του Λάνγκερχανς είναι περιοχές του παγκρέατος που περιέχουν τα ενδοκρινικά κύτταρα (που παράγουν ορμόνες), που ανακαλύφθηκαν το 1869 από τον Γερμανό παθολογοανατόμο Πάουλ Λάνγκερχανς.[1] Οι νησίδες αποτελούν το 1-2% του όγκου του παγκρέατος και δέχονται 10-15% της ροής του αίματος.[2][3] Οι νησίδες είναι διατεταγμένες σε πυκνώματα σε όλο το ανθρώπινο πάγκρεας και διαδραματίζουν σημαντικότατο ρόλο στον μεταβολισμό της γλυκόζης .[4]
Δομή
[Επεξεργασία | επεξεργασία κώδικα]Υπάρχουν περίπου ένα εκατομμύριο νησίδια που διανέμονται με τη μορφή πυκνωμάτων σε ολόκληρο το πάγκρεας υγιούς ενήλικου ανθρώπου, καθεμία από τις οποίες έχει κατά μέσον όρο διάμετρο περίπου 0,2 mm.[5] : 928 Κάθε μία χωρίζεται από τον περιβάλλοντα παγκρεατικό ιστό με λεπτή ινώδη κάψουλα συνδετικού ιστού, συνεχόμενη με τον ινώδη συνδετικό ιστό που είναι συνυφασμένος σε όλο το υπόλοιπο του παγκρέατος. : 928
Μικροανατομία
[Επεξεργασία | επεξεργασία κώδικα]Οι ορμόνες που παράγονται στα νησίδια του παγκρέατος εκκρίνονται απευθείας στη ροή του αίματος από (τουλάχιστον) πέντε τύπους κυττάρων. Στις νησίδες των αρουραίων, υποσύνολα ενδοκρινικών κυττάρων κατανέμονται ως εξής:[6]
- Κύτταρα άλφα που παράγουν γλυκαγόνη (20% των συνολικών νησιδίων)
- Κύτταρα βήτα, που παράγουν ινσουλίνη και αμυλίνη (≈70%)
- Κύτταρα δέλτα, που παράγουν σωματοστατίνη (<10%)
- Κύτταρα έψιλον που παράγουν γκρελίνη (<1%)
- Κύτταρα PP (κύτταρα γάμμα ή κύτταρα F) που παράγουν παγκρεατικό πολυπεπτίδιο (<5%)
Έχει αναγνωριστεί ότι η κυτοαρχιτεκτονική των παγκρεατικών νησιδίων διαφέρει μεταξύ των ειδών.[7][8][9] Συγκεκριμένα, ενώ τα νησίδια των τρωκτικών χαρακτηρίζονται από κυρίαρχο ποσοστό β-κυττάρων που παράγουν ινσουλίνη στον πυρήνα του συμπλέγματος και από σπάνια κύτταρα άλφα, δέλτα και ΡΡ στην περιφέρεια, τα ανθρώπινα νησίδια εμφανίζουν κύτταρα άλφα και βήτα σε στενή σχέση μεταξύ τους σε όλο το σύμπλεγμα.
Το ποσοστό των β-κυττάρων στα νησίδια ποικίλλει ανάλογα με το είδος, στους ανθρώπους είναι περίπου 40-50%. Εκτός από τα ενδοκρινικά κύτταρα, υπάρχουν υποστηρικτικά κύτταρα (ινοβλάστες), αγγειακά κύτταρα (ενδοθηλιακά κύτταρα, περικύτταρα), ανοσοκύτταρα (κοκκιοκύτταρα, λεμφοκύτταρα, μακροφάγα, δενδριτικά κύτταρα) ή νευρικά κύτταρα.[10]
Μεγάλη ποσότητα αίματος ρέει μέσω των νησίδων, 5-6 ml / min ανά 1 g νησιδίου. Είναι έως και 15 φορές περισσότερο από ό, τι στον εξωκρινικό ιστό του παγκρέατος.[10]
Τα νησιδια μπορούν να επηρεάσουν το ένα το άλλο μέσω της παρακρίνης και της αυτοκρινούς επικοινωνίας, και τα βήτα κύτταρα συνδέονται ηλεκτρικά με έξι έως επτά άλλα βήτα κύτταρα (αλλά όχι σε άλλους τύπους κυττάρων).[11]
-
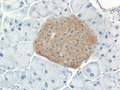
Παγκρεατικό νησίδιο με χρώση
-
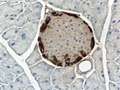
Παγκρεατικό νησίδιο. Εμφαίνονται τα άλφα κύτταρα
-
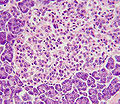
Παγκρεατικό νησίδιο. Εμφαίνονται τα βήτα κύτταρα.
Λειτουργία
[Επεξεργασία | επεξεργασία κώδικα]Το σύστημα ανατροφοδότησης παρακρίνης των παγκρεατικών νησίδων έχει την ακόλουθη δομή:[12]
- Γλυκόζη / Ινσουλίνη: ενεργοποιεί τα βήτα κύτταρα και αναστέλλει τα άλφα κύτταρα
- Γλυκογόνο / Γλυκαγόνο: ενεργοποιεί τα άλφα κύτταρα που ενεργοποιούν τα βήτα κύτταρα και τα δέλτα κύτταρα
- Σωματοστατίνη: αναστέλλει τα άλφα κύτταρα και τα βήτα κύτταρα
Ένας μεγάλος αριθμός υποδοχέων συζευγμένων με πρωτεΐνη G (GPCRs) ρυθμίζουν την έκκριση ινσουλίνης, γλυκαγόνης και σωματοστατίνης από παγκρεατικά νησίδια,[13] και μερικά από αυτούς τους GPCRs είναι στόχοι φαρμάκων που χρησιμοποιούνται για τη θεραπεία του διαβήτη τύπου 2 (αναφ. GLP-1 αγωνιστές υποδοχέων, αναστολείς DPPIV).
-
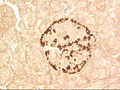
Νησίδιο ποντικού ανοσοχρωματισμένο για παγκρεατικό πολυπεπτίδιο
-
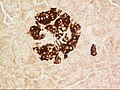
Νησίδιο ποντικού ανοσοχρωματισμένο για ινσουλίνη
-
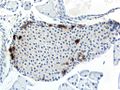
Νησίδιο ποντικού ανοσοχρωματισμένο για γλυκαγόνη
Ηλεκτρική δραστηριότητα
[Επεξεργασία | επεξεργασία κώδικα]Η ηλεκτρική δραστηριότητα των παγκρεατικών νησίδων έχει μελετηθεί χρησιμοποιώντας τεχνικές σφιγκτήρα τμήματος (τεχνική που αποκαλείται "patch clamp"). Αποδείχθηκε ότι η συμπεριφορά των κυττάρων σε ανέπαφες νησίδες διαφέρει σημαντικά από τη συμπεριφορά των διεσπαρμένων κυττάρων.[14]
Κλινική σημασία
[Επεξεργασία | επεξεργασία κώδικα]Διαβήτης
[Επεξεργασία | επεξεργασία κώδικα]Τα βήτα κύτταρα των παγκρεατικών νησίδων εκκρίνουν ινσουλίνη και έτσι διαδραματίζουν σημαντικό ρόλο στον διαβήτη . Πιστεύεται ότι καταστρέφονται από ανοσολογικές επιθέσεις. Ωστόσο, υπάρχουν επίσης ενδείξεις ότι τα βήτα κύτταρα δεν έχουν καταστραφεί, αλλά έχουν μόνο καταστεί μη λειτουργικά.
Μεταμόσχευση
[Επεξεργασία | επεξεργασία κώδικα]Επειδή τα βήτα κύτταρα στα παγκρεατικά νησίδια καταστρέφονται επιλεκτικά από μια αυτοάνοση διαδικασία στον διαβήτη τύπου 1, οι κλινικοί γιατροί και οι ερευνητές επιδιώκουν ενεργά τη μεταμόσχευση νησιδίου ως μέσου αποκατάστασης της φυσιολογικής λειτουργίας των β-κυττάρων, η οποία θα προσφέρει εναλλακτική λύση σε μια πλήρη μεταμόσχευση παγκρέατος ή τεχνητό πάγκρεας .[15][16] Η μεταμόσχευση νησιδίου προέκυψε ως βιώσιμη επιλογή για τη θεραπεία με ινσουλίνη που απαιτεί ο διαβήτησ στις αρχές της δεκαετίας του 1970 με σταθερή πρόοδο τις τελευταίες τρεις δεκαετίες.[17] Πρόσφατες κλινικές δοκιμές έδειξαν ότι η ανεξαρτησία της ινσουλίνης και ο βελτιωμένος μεταβολικός έλεγχος μπορούν να επιτευχθούν αναπαραγώγιμα μετά τη μεταμόσχευση νησίδων από νεκρό ανθρώπινο σώμα σε ασθενείς με ασταθή διαβήτη τύπου 1 .
Τα άτομα με υψηλό ΔΜΣ είναι ακατάλληλοι δότες παγκρέατος λόγω μεγαλύτερων τεχνικών επιπλοκών κατά τη μεταμόσχευση. Ωστόσο, είναι δυνατόν να απομονωθεί ένας μεγαλύτερος αριθμός νησίδων λόγω του μεγαλύτερου παγκρέατός τους, και επομένως είναι πιο κατάλληλοι δότες νησίδων.[18]
Η μεταμόσχευση νησιδίων περιλαμβάνει μόνον τη μεταφορά ιστού που αποτελείται από βήτα κύτταρα που είναι απαραίτητα ως θεραπεία αυτής της ασθένειας. Αποτελεί, έτσι, πλεονέκτημα έναντι της μεταμόσχευσης ολόκληρου του παγκρέατος, το οποίο είναι πιο τεχνικά απαιτητικό και ενέχει κίνδυνο, για παράδειγμα, παγκρεατίτιδας που οδηγεί σε απώλεια οργάνων.[18] Ένα άλλο πλεονέκτημα είναι ότι οι ασθενείς δεν χρειάζονται γενική αναισθησία.[19]
Η μεταμόσχευση νησίδων για διαβήτη τύπου 1 απαιτεί επί του παρόντος ισχυρή ανοσοκαταστολή για να αποφευχθεί η απόρριψη ξενιστή από δότες νησίδων.[20]
Οι νησίδες μεταμοσχεύονται σε μια πύλη φλέβα, η οποία στη συνέχεια εμφυτεύεται στο ήπαρ.[18] Υπάρχει κίνδυνος θρόμβωσης της πύλης του φλεβικού κλάδου και της χαμηλής τιμής της επιβίωσης της νησίδας λίγα λεπτά μετά τη μεταμόσχευση, επειδή η αγγειακή πυκνότητα σε αυτό το σημείο είναι μετά τη χειρουργική επέμβαση αρκετά χαμηλότερη από ό, τι στα ενδογενή νησίδια. Έτσι, η νεοαγγείωση είναι το κλειδί για την επιβίωση νησίδων, που υποστηρίζεται, για παράδειγμα, από VEGF που παράγεται από νησίδες και αγγειακά ενδοθηλιακά κύτταρα.[10][19] Ωστόσο, η ενδοπορική μεταμόσχευση έχει κάποιες άλλες αδυναμίες, και έτσι εξετάζονται άλλες εναλλακτικές θέσεις που θα παρέχουν καλύτερο μικροπεριβάλλον για την εμφύτευση νησίδων. Η έρευνα για τη μεταμόσχευση νησιδίων επικεντρώνεται επίσης στην ενθυλάκωση νησιού, στην ανοσοκαταστολή χωρίς CNI (αναστολέας καλσινευρίνης), στους βιοδείκτες βλάβης της νησίδας ή στην έλλειψη δότη.[21]
Εναλλακτική πηγή β-κυττάρων, όπως τα κύτταρα που παράγουν ινσουλίνη προέρχονται από ενήλικα βλαστικά κύτταρα ή προγονικά κύτταρα, τα οποία θα συνέβαλλαν στην αντιμετώπιση της έλλειψης δότη για μεταμόσχευση. Ο τομέας της αναγεννητικής ιατρικής εξελίσσεται γρήγορα και προσφέρει μεγάλη ελπίδα για το εγγύς μέλλον. Ωστόσο, ο διαβήτης τύπου 1 είναι το αποτέλεσμα της αυτοάνοσης καταστροφής των β-κυττάρων στο πάγκρεας. Επομένως, αποτελεσματική θεραπεία θα απαιτήσει διαδοχική, ολοκληρωμένη προσέγγιση που θα συνδυάζει επαρκείς και ασφαλείς ανοσολογικές παρεμβάσεις με αναγεννητικές προσεγγίσεις βήτα κυττάρων.[22] Έχει επίσης αποδειχθεί ότι τα άλφα κύτταρα μπορούν να αλλάξουν αυθόρμητα και να διαφοροποιηθούν σε βήτα κύτταρα παγκρεατικές νησίδες τόσο σε υγιή άτομα όσο και σε διαβητικούς ανθρώπους αλλά και ποντικούς, μια πιθανή μελλοντική πηγή αναγέννησης βήτα κυττάρων.[23] Στην πραγματικότητα, έχει βρεθεί ότι η μορφολογία των νησίδων και η ενδοκρινική διαφοροποίηση σχετίζονται άμεσα.[24] Τα ενδοκρινικά προγονικά κύτταρα διαφοροποιούνται μεταναστεύοντας στη συνοχή και σχηματίζοντας πρόδρομους νησίδες που μοιάζουν με μπουμπούκια, ή "χερσονήσους", όπου τα άλφα κύτταρα αποτελούν το εξωτερικό στρώμα της "χερσονήσου" και τα βήτα κύτταρα σχηματίζονται αργότερα κάτω από αυτά.
Πρόσθετες εικόνες
[Επεξεργασία | επεξεργασία κώδικα]-
Παγκρεατικές νησίδες, ο ελαφρύτερος ιστός μεταξύ του πιο σκούρου, κυψελιδικού παγκρεατικού ιστού, χρώση με h - e
-
Απεικόνιση του παγκρέατος σκυλιών. 250 Χ.
-
Διαρθρωτικές διαφορές μεταξύ νησίδων αρουραίου (άνω) και νησιωτικών νησίδων (κάτω) καθώς και του κοιλιακού τμήματος (αριστερά) και του ραχιαίου τμήματος (δεξιά) του παγκρέατος . Διαφορετικοί τύποι κυττάρων κωδικοποιούνται με χρώμα. Τα νησίιδια τρωκτικών, σε αντίθεση με τα ανθρώπινα, παρουσιάζουν τον χαρακτηριστικό πυρήνα ινσουλίνης.
Παραπομπές
[Επεξεργασία | επεξεργασία κώδικα]- ↑ Langerhans P (1869). «Beitrage zur mikroscopischen anatomie der bauchspeichel druse». Inaugural-dissertation. Berlin: Gustav Lange.
- ↑ Ganong's review of medical physiology (23 έκδοση). McGraw Hill Medical. 22 Ιουλίου 2009. σελ. 316. ISBN 978-0-07-160568-7.
- ↑ «Functional Anatomy of the Endocrine Pancreas». Αρχειοθετήθηκε από το πρωτότυπο στις 31 Μαρτίου 2023. Ανακτήθηκε στις 10 Μαΐου 2021.
- ↑ Pour, Parviz M.; Standop, Jens; Batra, Surinder K. (January 2002). «Are islet cells the gatekeepers of the pancreas?». Pancreatology 2 (5): 440–448. doi:. PMID 12378111.
- ↑ Sleisenger, edited by Mark Feldman, Lawrence S. Friedman, Lawrence J. Brandt; consulting editor, Marvin H. (2015). Sleisenger & Fordtran's gastrointestinal and liver disease pathophysiology, diagnosis, management (10th έκδοση). St. Louis, Missouri: Elsevier Health Sciences. ISBN 978-1-4557-4989-8.
- ↑ Elayat AA; el-Naggar MM; Tahir M; Bassam dahrouj (1995). «An immunocytochemical and morphometric study of the rat pancreatic islets». Journal of Anatomy. 186 (Pt 3) (Pt 3): 629–37. PMID 7559135.
- ↑ «Assessment of human pancreatic islet architecture and composition by laser scanning confocal microscopy». Journal of Histochemistry and Cytochemistry 53 (9): 1087–97. 2005. doi:. PMID 15923354.
- ↑ «A novel method for the assessment of cellular composition and beta-cell viability in human islet preparations». American Journal of Transplantation 5 (7): 1635–45. 2005. doi:. PMID 15943621.
- ↑ «The unique cytoarchitecture of human pancreatic islets has implications for islet cell function». Proceedings of the National Academy of Sciences of the United States of America 103 (7): 2334–9. 2006. doi:. ISSN 1091-6490. PMID 16461897. Bibcode: 2006PNAS..103.2334C.
- ↑ 10,0 10,1 10,2 Jansson, Leif; Barbu, Andreea; Bodin, Birgitta; Drott, Carl Johan; Espes, Daniel; Gao, Xiang; Grapensparr, Liza; Källskog, Örjan και άλλοι. (2016-04-02). «Pancreatic islet blood flow and its measurement» (στα αγγλικά). Upsala Journal of Medical Sciences 121 (2): 81–95. doi:. ISSN 0300-9734. PMID 27124642.
- ↑ Kelly, Catriona; McClenaghan, Neville H.; Flatt, Peter R. (2011). «Role of islet structure and cellular interactions in the control of insulin secretion». Islets 3 (2): 41–47. doi:. PMID 21372635.
- ↑ Wang, Michael B.· Bullock, John (2001). Physiology. Hagerstown, MD: Lippincott Williams & Wilkins. σελ. 391. ISBN 978-0-683-30603-3.
- ↑ Amisten, S; Salehi, A; Rorsman, P; Jones, PM; Persaud, SJ (2013). «An atlas and functional analysis of G-protein coupled receptors in human islets of Langerhans». Pharmacol Ther 139 (3): 359–91. doi:. PMID 23694765.
- ↑ «Biophysical properties of gap junctions between freshly dispersed pairs of mouse pancreatic beta cells». Biophysical Journal 59 (1): 76–92. 1991. doi:. PMID 2015391. PMC 1281120. Bibcode: 1991BpJ....59...76P. https://archive.org/details/sim_biophysical-journal_1991-01_59_1/page/76.
- ↑ Meloche RM (2007). «Transplantation for the treatment of type 1 diabetes». World Journal of Gastroenterology 13 (47): 6347–55. doi:. PMID 18081223.
- ↑ «Transplantation: current developments and future directions; the future of clinical islet transplantation as a cure for diabetes». Frontiers in Bioscience 13 (13): 1192–205. 2008. doi:. PMID 17981623.
- ↑ «25 Years of the Ricordi Automated Method for Islet Isolation». CellR4 1 (1): 8–22. 2013. PMID 30505878. PMC 6267808. http://www.cellr4.org/article/128.
- ↑ 18,0 18,1 18,2 Niclauss, Nadja; Meier, Raphael; Bédat, Benoît; Berishvili, Ekaterine; Berney, Thierry (2016-01-27), Stettler, C.; Christ, E.; Diem, P., επιμ., «Beta-Cell Replacement: Pancreas and Islet Cell Transplantation», Endocrine Development (S. Karger AG) 31: 146–162, doi:, ISBN 978-3-318-05638-9, PMID 26824893, https://www.karger.com/Article/FullText/439412, ανακτήθηκε στις 2020-09-11
- ↑ 19,0 19,1 Gamble, Anissa; Pepper, Andrew R.; Bruni, Antonio; Shapiro, A. M. James (2018-03-04). «The journey of islet cell transplantation and future development». Islets 10 (2): 80–94. doi:. ISSN 1938-2014. PMID 29394145.
- ↑ Chatenoud L (2008). «Chemical immunosuppression in islet transplantation—friend or foe?». New England Journal of Medicine 358 (11): 1192–3. doi:. ISSN 0028-4793. PMID 18337609.
- ↑ Chang, Charles A.; Lawrence, Michael C.; Naziruddin, Bashoo (October 2017). «Current issues in allogeneic islet transplantation». Current Opinion in Organ Transplantation 22 (5): 437–443. doi:. ISSN 1087-2418. PMID 28692442.
- ↑ «Overcoming the challenges now limiting islet transplantation: a sequential, integrated approach». Annals of the New York Academy of Sciences 1079 (1): 383–98. 2006. doi:. ISSN 0077-8923. PMID 17130583. Bibcode: 2006NYASA1079..383P.
- ↑ van der Meulen, T.; Mawla, A.M.; DiGruccio, M.R.; Adams, M.W.; Nies, V.; Dolleman, S.; Liu, S.; Ackermann, A.M. και άλλοι. (2017). «Virgin Beta Cells Persist throughout Life at a Neogenic Niche within Pancreatic Islets». Cell Metabolism 25 (4): 911–926. doi:. PMID 28380380. http://www.escholarship.org/uc/item/85r6t1w6.
- ↑ Sharon, N.; Chawla, R.; Mueller, J.; Vanderhooft, J.; Whitehorn, L.J.; Rosenthal, B.; Gürtler, M.; Estanboulieh, R.R. και άλλοι. (2019). «A Peninsular Structure Coordinates Asynchronous Differentiation with Morphogenesis to Generate Pancreatic Islets». Cell 176 (4): 790–804.e13. doi:. ISSN 0092-8674. PMID 30661759.
Εξωτερικοί σύνδεσμοι
[Επεξεργασία | επεξεργασία κώδικα]- Πάγκρεας στον ανθρώπινο άτλαντα πρωτεϊνών