Vindolin
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
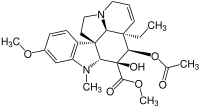
| ||||||||||
| Allgemeines | ||||||||||
| Name | Vindolin | |||||||||
| Summenformel | C25H32N2O6 | |||||||||
| Kurzbeschreibung |
weißer bis gelblicher, kristalliner Feststoff[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 456,54 g·mol−1 | |||||||||
| Aggregatzustand |
fest[1] | |||||||||
| Dichte |
1,33 g·cm−3[2] | |||||||||
| Schmelzpunkt | ||||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||
Vindolin ist eine natürlich vorkommende chemische Verbindung und gehört zur Gruppe der Alkaloide, genauer der Vincaalkaloide beziehungsweise Catharanthus-Alkaloide.
Vorkommen
[Bearbeiten | Quelltext bearbeiten]
Vindolin ist eines der mengenmäßig wichtigeren Alkaloide in der Rosafarbenen Catharanthe, einer Pflanze aus Madagaskar, die über 100 verschiedene Alkaloide bildet.[3][4] Vindolin ist außerdem ein Strukturelement des Alkaloids Vinblastin, das in der gleichen Pflanze in geringen Mengen vorkommt.[3]
Biosynthese
[Bearbeiten | Quelltext bearbeiten]Die Biosynthese verläuft über Strictosidin, das aus Secologanin und Tryptamin gebildet wird. Strictosidin wiederum wird in Tabersonin und von dort über sieben Schritte in Vindolin umgewandelt. Strictosidin ist auch der Vorläufer von Catharanthin, das neben Vindolin die zweite Komponente in Vinblastin und Vincristin ist.[5]
Synthese
[Bearbeiten | Quelltext bearbeiten]Mehrere Totalsynthesen des Vindolins sind bekannt.[6][7]
Reaktionen und Verwendung
[Bearbeiten | Quelltext bearbeiten]Vindolin dient als Edukt für die Synthese des Krebsmedikaments Vinorelbin.[8]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c Eintrag zu Vindoline, bei TCI Europe, abgerufen am 14. Juli 2024.
- ↑ a b c Santa Cruz Biotechnology: Vindoline | CAS 2182-14-1 | SCBT - Santa Cruz Biotechnology, abgerufen am: 14. Juli 2024.
- ↑ a b Gordon M. Cragg, David G. I. Kingston, David J. Newman: Anticancer Agents from Natural Products. CRC Press, 2011, ISBN 978-1-4398-1383-6, S. 180.
- ↑ Yongliang Liu, Barunava Patra, Sitakanta Pattanaik, Ying Wang, Ling Yuan: GATA and Phytochrome Interacting Factor Transcription Factors Regulate Light-Induced Vindoline Biosynthesis in Catharanthus roseus. In: Plant Physiology. Band 180, Nr. 3, Juli 2019, S. 1336–1350, doi:10.1104/pp.19.00489, PMID 31123092, PMC 6752914 (freier Volltext).
- ↑ Yongliang Liu, Barunava Patra, Sitakanta Pattanaik, Ying Wang, Ling Yuan: GATA and Phytochrome Interacting Factor Transcription Factors Regulate Light-Induced Vindoline Biosynthesis in Catharanthus roseus. In: Plant Physiology. Band 180, Nr. 3, Juli 2019, S. 1336–1350, doi:10.1104/pp.19.00489, PMID 31123092, PMC 6752914 (freier Volltext) – (Supplemental Data, Supplemental Figure S1).
- ↑ Daisuke Kato, Yoshikazu Sasaki, Dale L. Boger: Asymmetric Total Synthesis of Vindoline. In: Journal of the American Chemical Society. Band 132, Nr. 11, 24. März 2010, S. 3685–3687, doi:10.1021/ja910695e, PMID 20187641, PMC 2854892 (freier Volltext).
- ↑ Masayoshi Ando, George Buechi, Takeshi Ohnuma: Total synthesis of (±)-vindoline. In: Journal of the American Chemical Society. Band 97, Nr. 23, November 1975, S. 6880–6881, doi:10.1021/ja00856a056.
- ↑ Alain Duflos, Anna Kruczynski, Jean-Marc Barret: Novel Aspects of Natural and Modified Vinca Alkaloids. In: Current Medicinal Chemistry - Anti-Cancer Agents. Band 2, Nr. 1, S. 55–70, doi:10.2174/1568011023354452.
