Silber(I)-fluorid
Silber(I)-fluorid ist das Silbersalz der Flusssäure (Fluorwasserstoffsäure). Im Gegensatz zu den anderen Halogeniden des Silbers ist es weniger lichtempfindlich, sehr gut in Wasser löslich und hygroskopisch.
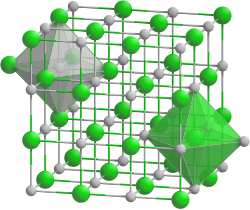
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||
| _ Ag+ _ F− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Silber(I)-fluorid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Verhältnisformel | AgF | |||||||||||||||
| Kurzbeschreibung |
gelber Feststoff[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 126,87 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte | ||||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
1150 °C[2] | |||||||||||||||
| Löslichkeit |
sehr gut in Wasser (etwa 1820 g·l−1 bei 15,5 °C)[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| MAK |
0,01 mg·m−3[2] | |||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
−204,6 kJ/mol[3] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Gewinnung und Darstellung
BearbeitenDas Silber(I)-fluorid kann sowohl aus den Elementen Silber und Fluor als auch aus Silber(I/III)-oxid (AgO), Silber(I)-oxid (Ag2O) und Silber(I)-carbonat (Ag2CO3) jeweils mit Fluorwasserstoff erhalten werden:[4]
- Silber(I)-oxid reagiert mit Fluorwasserstoff zu Silber(I)-fluorid und Wasser.
Eigenschaften
BearbeitenWie Silberchlorid und Silberbromid kristallisiert auch Silber(I)-fluorid in der kubischen NaCl-Struktur. Im Gegensatz zu den anderen Silberhalogeniden kann AgF aus wässrigen Lösungen als verschiedene Hydrate kristallisieren (AgF · H2O, AgF · 2 H2O und AgF · 4 H2O). Mit überschüssiger Fluorwasserstoffsäure bilden sich AgF · HF und AgF · 3 HF. In einem Liter Wasser lösen sich bei Raumtemperatur (25 °C) 1,8 kg AgF, wobei Silber(I)-fluorid in Silber- und Fluoridionen dissoziiert:
Die Bildungsenthalpie aus den Elementen (∆Hf) beträgt −204 kJ.
Verwendung
BearbeitenSilber(I)-fluorid wird in der Analogfotografie angewendet, wobei Farbfilme mit dem besonders im UV-Bereich empfindlichen AgF beschichtet werden.[5] Silber(I)-fluorid dient als mildes Fluoridierungsmittel für Elementhalogenide und bei der Herstellung von Organofluorverbindungen durch Addition von Fluor an Doppelbindungen. Als Beispiel sei die Anlagerung von AgF an Perfluoralkene in Acetonitril erwähnt, bei der Perfluoralkylsilber(I)-Verbindungen entstehen: R–CF=CF2 + AgF → R–(CF–CF3)Ag.[6]
Auch bei der Behandlung von Karies wird AgF oder dessen Diamminkomplex unter dem Namen Saforide eingesetzt (siehe Weblinks).
Sicherheitshinweise
BearbeitenDie Handhabung von Silber(I)-fluorid ist nicht ungefährlich, da es beispielsweise mit Silicium, Titan und Calciumhydrid unter starker Hitzeentwicklung reagiert. Bei Kontakt mit Bor und Natrium besteht sogar Explosionsgefahr. Des Weiteren wirkt es ätzend auf Augen und Haut bzw. bei Einatmung in die Lunge.[2]
Siehe auch
BearbeitenWeblinks
BearbeitenEinzelnachweise
Bearbeiten- ↑ A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1344.
- ↑ a b c d e f g h Eintrag zu Silber(I)-fluorid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 9. Januar 2019. (JavaScript erforderlich)
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-4.
- ↑ Georg Brauer (Hrsg.): Handbook of Preparative Inorganic Chemistry. 2. Auflage. Band 1. Academic Press, New York 1963, S. 240 (sciencemadness.org [PDF]).
- ↑ Norman N. Greenwood, Alan Earnshaw: Chemie der Elemente. 1., korrigierte Auflage. VCH-Verlag, Weinheim 1990, ISBN 3-527-26169-9, S. 1516.
- ↑ William T. Miller, Robert J. Burnard: Perfluoroalkylsilver compounds. In: Journal of the American Chemical Society. Band 90, 1968, S. 7367–7368, doi:10.1021/ja01028a047.

