Carbazool
| Carbazool | |||||
|---|---|---|---|---|---|
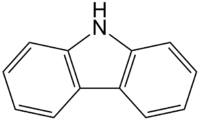
| Structuurformule en molecuulmodel | |||||
| |||||
Structuurformule van carbazool
| |||||
| Algemeen | |||||
| Molecuulformule | C12H9N | ||||
| IUPAC-naam | 9H-carbazool | ||||
| Andere namen | 9-azafluoreen, dibenzopyrrool, difenyleenimine, difenyleenimide, USAF EK-600 | ||||
| Molmassa | 167,206 g/mol | ||||
| SMILES | c1ccc2c(c1)c3ccccc3[nH]2
| ||||
| InChI | 1/C12H9N/c1-3-7-11-9(5-1)10-6-2-4-8-12(10)13-11/h1-8,13H
| ||||
| CAS-nummer | 86-74-8 | ||||
| PubChem | 6854 | ||||
| Wikidata | Q424003 | ||||
| Waarschuwingen en veiligheidsmaatregelen | |||||
| |||||
| H-zinnen | H301 - H315 - H319 - H335 - H351 - H400[1] | ||||
| EUH-zinnen | geen | ||||
| P-zinnen | P261 - P273 - P281 - P301+P310 - P305+P351+P338[1] | ||||
| Fysische eigenschappen | |||||
| Dichtheid | 1,301 g/cm³ | ||||
| Smeltpunt | 246,3[2] °C | ||||
| Kookpunt | 354,69[2] °C | ||||
| Vlampunt | 220[2] °C | ||||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | |||||
| |||||
Carbazool is een heterocyclische aromatische verbinding met als brutoformule C12H9N. De molecule bestaat uit drie ringen, een centrale pyrroolring, met aan weerszijden een benzeenring. Deze structuur vormt de achtergrond van de verouderde naam dibenzopyrrool. De gelijkenis met fluoreen, waarin het koolstofatoom op plaats 9 vervangen is door een stikstofatoom, ligt ten grondslag aan de (ook verouderde) naam 9-azafluoreen.
Synthese
[bewerken | brontekst bewerken]Voor de synthese van carbazool zijn verschillende manieren beschreven.
Borsche-Drechsel-cyclisatie
[bewerken | brontekst bewerken]Een klassieke synthese van carbazool is de Borsche-Drechsel-cyclisatie:[3][4]

In de eerste reactiestap wordt met behulp van fenylhydrazine het fenylhydrazon van cyclohexanon bereid. De tweede stap bestaat uit een door waterstofchloride gekatalyseerde omlegging en ringsluiting tot tetrahydrocarbazool. Door de reactie in azijnzuur uit te voeren zijn deze twee stappen tot een one-pot-reactie te combineren.[5][6] De laatste stap van de synthese betreft de oxidatie van de tetrahydroverbinding door loodmenie tot carbazool.
Methode volgens Graebe en Ullmann
[bewerken | brontekst bewerken]Een andere methode is die van Graebe en Ullmann:

In de eerste stap van deze synthese wordt een N-fenyl-1,2-diaminobenzeen omgezet in zijn diazoniumzout dat direct tot een 1,2,3-triazool reageert. Bij verhoogde temperatuur vormt dit, onder uitstoting van stikstofgas, carbazool.[7][8][9]
Bucherer-carbazoolsynthese
[bewerken | brontekst bewerken]Een derde synthetische benadering is die van Bucherer. In de Bucherer-carbazoolsynthese worden carbazoolderivaten (3) bereid uit naftolen (1) en arylhydrazines (2) met natriumwaterstofsulfiet als katalysator.[10] De studie naar het mechanisme van deze reactie, waarbij ook de isoleerbare intermediairen onderzocht werden, dateert van 1967.[11]

De reactie werd voor het eerst beschreven in 1908 door de Duitse scheikundige Hans Bucherer. Mechanistisch gezien is ze verwant aan de door dezelfde scheikundige ontwikkelde Bucherer-reactie.
Eigenschappen
[bewerken | brontekst bewerken]Het waterstofatoom aan stikstof is vrij zuur. In syntheses kan het door reactie met een sterke base vervangen worden door onder ander kalium, waarbij kaliumcarbazolaat ontstaat. Dit zout kan vervolgens omgezet worden in N-gesubstitueerde derivaten.[12]
Toepassingen
[bewerken | brontekst bewerken]Carbazool wordt toegepast in de synthese van dioxazineviolet (het Pigment Violet 23) en N-ethylcarbazool.
Derivaten van carbazool worden voor diverse doeleinden onderzocht en toegepast. N-ethylcarbazool wordt bestudeerd als drager voor waterstofopslag in auto's.[13][14] Een ander, het polymeer van N-vinylcarbazool, wordt toegepast als geleidend polymeer in het lichtgevoelige deel van fotokopieerapparatuur.[15] Onder invloed van gammastraling treedt polymerisatie op in de vaste stof.[16]
Verwante aromatische verbindingen
[bewerken | brontekst bewerken]- Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Carbozole op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
- Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Carbozol op de Duitstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
- ↑ a b c Productinformatie in de Online catalogus van Sigma Aldrich, geraadpleegd op 21 mei 2013.
- ↑ a b c . (2007). GEEN TITEL OPGEGEVEN Ed.: David R. Lide CRC Handbook of Chemistry and Physics (88th ed.) pag.: 3–86 – CRC Press ISBN 978-0-8493-0488-0
- ↑ W. Borsche, A. Witte, W. Bothe. (1908). Ueber Tetra- und Hexahydrocarbazolverbindungen und eine neue Carbazolsynthese Justus Liebig's Annalen der Chemie. 359 (1 - 2): pag.: 49–80 DOI:10.1002/jlac.19083590103
- ↑ E. Drechsel. (1888). Ueber Elektrolyse des Phenols mit Wechselströmen Journal für praktische Chemie. 38 (1): pag.: 65–74 DOI:10.1002/prac.18880380105
- ↑ Crosby U. Rogers, B. B. Corson. (1963). 1,2,3,4-TETRAHYDROCARBAZOLE25 mei 2013 Organic Syntheses. pag.: 884 Collective volume 4 geraadpleegd op 25 mei 2013
- ↑ Crosby U. Rogers, B. B. Corson. (1950). 1,2,3,4-TETRAHYDROCARBAZOLE25 mei 2013 Organic Syntheses. 30 pag.: 90 geraadpleegd op 25 mei 2013. Gearchiveerd op 7 februari 2012.
- ↑ . Overzicht van de Graebe-Ullmann reactie25 mei 2013 Internetpagina: Overzicht van de Graebe-Ullmann reactie geraadpleegd op 25 mei 2013
- ↑ Carl Graebe, Fritz Ullmann. (1896). Ueber eine neue Carbazolsynthese Justus Liebig's Annalen der Chemie. 291 (1): pag.: 16–17 DOI:10.1002/jlac.18962910104
- ↑ O. Bremer. (1934). Über die Bedeutung der Graebe-Ullmannschen Carbazolsynthese und deren Übertragung auf N-substituierte Pyridino-triazole Justus Liebig's Annalen der Chemie. 514 pag.: 279–291 DOI:10.1002/jlac.19345140116
- ↑ H Bucherer, F Seyde. (1908). GEEN TITEL OPGEGEVEN J prakt Chem. 77 pag.: 403
- ↑ Dr. Habil. H. Seeboth. (1967). The Bucherer Reaction and the Preparative Use of its Intermediate Products Angewandte Chemie International Edition in English. 6 (4): pag.: 307–317 DOI:10.1002/anie.196703071
- ↑ Gerd Collin, Hartmut Höke, Jörg Talbiersky. (2006). Carbazole Ullmann's Encyclopedia of Industrial Chemistry – Wiley-VCH Verlag GmbH & Co
- ↑ . Verwendung von Carbazol als Träger für Wasserstoff Elektor. Internetpagina: Verwendung von Carbazol als Träger für Wasserstoff
- ↑ . Alternativ-Kraftstoff Carbazol, Zaubersprit von der Zapfsäule27 mei 2013 Spiegel Online. Internetpagina: Alternativ-Kraftstoff Carbazol, Zaubersprit von der Zapfsäule geraadpleegd op 27 mei 2013
- ↑ G. Burton, J. Holman, J. Lazonby, G. Pilling, D. Waddington. GEEN TITEL OPGEGEVEN Chemical Storylines (2nd ed.) – Heinemann Educational Publishers ISBN 0-435-63119-5
- ↑ K. Tsutsui, K. Hirotsu, M. Umesaki, M. Kurahashi, A. Shimada, T. Higuchi. (1976). Structural chemistry of polymerizable monomers. I. Crystal structure of N-vinylcarbazole Acta Cryst.. B32 pag.: 3049–3053 DOI:10.1107/S0567740876009527


