Neomisin
Neomisin (neomisin) ialah antibiotik aminoglikosida yang memaparkan aktiviti bakteria terhadap basilus aerobik gram-negatif dan beberapa basilus anaerobik di mana rintangan masih belum timbul. Ia secara amnya tidak berkesan terhadap basilus gram-positif dan gram-negatif anaerobik. Neomisin datang dalam formulasi oral dan topikal, termasuk krim, salap, dan ubat mata. Neomisin tergolong dalam kelas antibiotik aminoglikosida yang mengandungi dua atau lebih gula amino yang disambungkan oleh ikatan glikosidik.
 | |
 | |
| Data klinikal | |
|---|---|
| Nama dagang | Neo-rx |
| AHFS/Drugs.com | Monograph |
| MedlinePlus | a682274 |
| Kaedah pemberian | Topikal, mulut |
| Kod ATC | |
| Status perundangan | |
| Status perundangan |
|
| Data farmakokinetik | |
| Bioketersediaan | Tiada |
| Pengikatan protein | N/A |
| Metabolisme | N/A |
| Penyingkiran separuh hayat | 2 ke 3 jam |
| Pengecam | |
| |
| Nombor CAS | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| ECHA InfoCard | 100.014.333 |
| Data kimia dan fizikal | |
| Formula | C23H46N6O13 |
| Jisim molar | 614.65 g·mol−1 |
| Model 3D (JSmol) | |
| |
| | |
Neomisin ditemui pada tahun 1949 oleh ahli mikrobiologi Selman Waksman dan pelajarnya Hubert Lechevalier di Universiti Rutgers. Neomisin menerima kelulusan untuk kegunaan perubatan pada tahun 1952.[1] Universiti Rutgers telah diberikan paten neomisin pada 1957.[2]
Penemuan
suntingNeomisin ditemui pada tahun 1949 oleh ahli mikrobiologi Selman Waksman dan pelajarnya Hubert Lechevalier di Universiti Rutgers. Ia dihasilkan secara semula jadi oleh bakteria Streptomyces fradiae.[3] Sintesis memerlukan keadaan nutrien tertentu sama ada dalam keadaan aerobik pegun atau tenggelam. Sebatian itu kemudiannya diperoleh dan ditulenkan daripada bakteria.[4]
Kegunaan perubatan
suntingNeomisin biasanya digunakan sebagai penyediaan topikal seperti Neosporin (neomisin/polymyxin B/bacitracin). Antibiotik juga boleh diberikan secara lisan, di mana ia biasanya digabungkan dengan antibiotik lain. Neomisin tidak diserap dari saluran gastrousus dan telah digunakan sebagai langkah pencegahan ensefalopati hepatik dan hiperkolesterolemia. Dengan membunuh bakteria dalam saluran usus, Neomisin mengekalkan paras ammonia yang rendah dan menghalang ensefalopati hepatik, terutamanya sebelum pembedahan gastrousus.[perlu rujukan]
Waksman dan Lechevalier pada asalnya menyatakan bahawa neomisin aktif terhadap bakteria tahan streptomisin serta Mycobacterium tuberculosis, agen penyebab tuberkulosis.[5] Neomisin juga telah digunakan untuk merawat pertumbuhan berlebihan bakteria usus kecil. Neomisin tidak diberikan melalui suntikan kerana ia sangat nefrotoksik (merosakkan fungsi buah pinggang), termasuk dalam kalangan aminoglikosida lain. Pengecualian diberi apabila neomisin dimasukkan dalam kuantiti yang kecil sebagai pengawet dalam sesetengah vaksin – biasanya 25 μg setiap dos.[6]
Spektrum
suntingSama seperti aminoglikosida lain, neomisin mempunyai aktiviti yang sangat baik terhadap bakteria gram-negatif, dan sebahagiannya berkesan terhadap bakteria gram-positif. Ia beracun kepada manusia secara relatif, dengan tindak balas alahan dicatatkan sebagai tindak balas buruk lazim (lihat: hipersensitiviti). Doktor kadangkala mengesyorkan menggunakan salap antibiotik tanpa neomisin seperti Polysporin.[7] Senarai berikut mewakili data kerentanan kepekatan perencatan minimum (MIC) bagi beberapa bakteria gram-negatif utama dalam perubatan.[8]
- Enterobacter cloacae : >16 μg/ml
- Escherichia coli : 1 μg/ml
- Proteus vulgaris : 0.25 μg/ml
Kesan sampingan
suntingPada 2005–06, Neomisin ialah alergen kelima paling lazim dalam keputusan ujian tampalan (10.0%).[9] Ia juga diketahui merupakan antagonis asid gama-aminobutirik (GABA), dan boleh membawa kepada sawan dan psikosis.[10] Seperti aminoglikosida lain, neomisin telah ditunjukkan sebagai ototoksik (membahayakan telinga), menyebabkan tinitus, kehilangan pendengaran dan masalah vestibular dalam sebilangan kecil pesakit.
Biologi molekul
suntingAktiviti
suntingAktiviti antibakteria Neomisin berpunca daripada pengikatan di subunit 30S ribosom prokariotik, di mana ia menghalang translasi mRNA prokariotik.[11]
Neomisin juga mempamerkan pertalian pengikatan tinggi terhadap fosfatidillinositol 4,5-bisfosfat (PIP2), komponen fosfolipid membran sel.[12]
Rintangan
suntingRintangan neomisin diberikan oleh salah satu daripada dua gen kanamisin kinase.[13] Gen yang memberikan rintangan neomisinbiasanya dimasukkan ke dalam plasmid DNA yang digunakan untuk mewujudkan turunan sel mamalia stabil yang menyatakan protein klon dalam kultur. Banyak plasmid ekspresi protein yang tersedia secara komersial mengandungi gen rintangan neo sebagai penanda boleh dipilih.
Laluan biosintetik
suntingNeomisin pertama kali diasingkan daripada Streptomyces fradiae dan Streptomyces albogriseus pada 1949 (NBRC 12773).[14] Neomisin ialah campuran neomisin B (framisetin); dan epimer neomisin C, komponen terakhir menyumbang kira-kira 5–15% daripada campuran. Ia adalah sebatian asas yang paling aktif dengan tindak balas alkali.[5] Ia juga stabil haba dan larut dalam air (sementara tidak larut dalam pelarut organik).[5] Neomisin mempunyai aktiviti yang baik terhadap bakteria gram-positif dan gram-negatif, tetapi bersifat ototoksik. Oleh itu, penggunaannya terhad kepada rawatan jangkitan usus melalui mulut.[15]
Neomisin A, juga dipanggil neamina, mengandungi D-neosamina dan 2-deoksistreptamina. Enam gen bertanggungjawab dalam biosintesis neamina: gen DOIS (btrC, neo7); L-glutamina: gen aminotransferase DOI (btrS, neo6); gen glikosiltransferase yang diduga (btrM, neo8); gen aminotransferase (serupa dengan glutamat-1-semialdehid 2,1-aminomutase) (btrB, neo18); gen alkohol dehidrogenase yang diduga (btrE, neo5); dan satu lagi gen dehidrogenase diduga (serupa dengan korina dehidrogenase dan flavoprotein berkaitan) (btrQ, neo11).[16] Deasetilase yang bertindak untuk mengeluarkan kumpulan asetil pada bahagian N-asetilglukosamina perantaraan aminoglikosida (Neo16) masih perlu dijelaskan (jujukan serupa dengan BtrD).[17]
Seterusnya ialah pelekatan D-ribose melalui ribosilasi neamina, menggunakan 5-fosforibosil-1-difosfat (PRPP) sebagai penderma ribosil (BtrL, BtrP);[18] glikosiltransferase (potensi homolog RibF, LivF, Parf) gen (Neo15).[19]
Neosamina B (L-neosamina B) berkemungkinan besar dibiosintesis dengan cara yang sama seperti neosamina C (D-niosamina) dalam biosintesis neamina, tetapi dengan langkah epimerisasi tambahan yang diperlukan untuk mengambil kira kehadiran epimer neosamina B dalam neomisin B.[20]
Neomisin C boleh menjalani sintesis enzimatik daripada ribostamisin.[21]
Komposisi
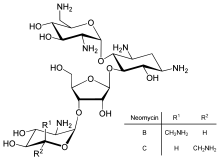
suntingNeomisin gred standard terdiri daripada beberapa sebatian berkaitan, termasuk neomisin A (neamina), neomisin B (framisetin), neomisin C, dan beberapa sebatian kecil yang terdapat dalam kuantiti yang jauh lebih rendah. Neomisin B ialah komponen paling aktif dalam neomisin, diikuti oleh neomisin C dan neomisin A. Neomisin A ialah produk degradasi tidak aktif bagi isomer C dan B.[22] Kuantiti komponen ini dalam neomisin berbeza bergantung pada pengilang dan proses pembuatan.[23]
Pengikatan DNA
suntingAminoglikosida seperti neomisin dikenali kerana keupayaannya untuk mengikat RNA dupleks dengan pertalian tinggi.[24] Pemalar perkaitan neomisin dengan RNA tapak A berada dalam julat 10 9 M−1.[25] Walau bagaimanapun, lebih daripada 50 tahun selepas penemuannya, sifat pengikat DNA-nya masih tidak diketahui. Neomisin telah ditunjukkan untuk mendorong penstabilan haba DNA tripleks, sementara mempunyai sedikit atau hampir tiada kesan pada penstabilan dupleks B-DNA.[26] Neomisin juga ditunjukkan untuk mengikat struktur yang menggunakan struktur bentuk A, DNA tripleks menjadi salah satu daripadanya. Neomisin juga termasuk pembentukan tripleks hibrid DNA:RNA.[27]
Rujukan
sunting- ^ Fischer J, Ganellin CR (2006). Analogue-based Drug Discovery (dalam bahasa Inggeris). John Wiley & Sons. m/s. 507. ISBN 9783527607495. Diarkibkan daripada yang asal pada 2020-08-01. Dicapai pada 2020-05-25.
- ^ US, "Neomycin and process of preparation"
- ^ "The Nobel Prize in Physiology or Medicine 1952". Nobel Foundation. Diarkibkan daripada yang asal pada 2018-06-19. Dicapai pada 2008-10-29.
- ^ "Neomycin". Pharmaceutical Manufacturing Encyclopedia. 3 (ed. 3rd). 2007. m/s. 2415–2416.
- ^ a b c "Neomycin, a New Antibiotic Active against Streptomycin-Resistant Bacteria, including Tuberculosis Organisms". Science. New York, N.Y. 109 (2830): 305–7. March 1949. Bibcode:1949Sci...109..305W. doi:10.1126/science.109.2830.305. PMID 17782716.
- ^ "Hypersensitivity reactions to vaccine components". Dermatitis. 16 (3): 115–20. September 2005. doi:10.1097/01206501-200509000-00004. PMID 16242081.
- ^ "Your Medicine Cabinet". DERMAdoctor.com, Inc. Diarkibkan daripada yang asal pada 2009-07-09. Dicapai pada 2008-10-19.
- ^ "Neomycin sulfate, EP Susceptibility and Minimum Inhibitory Concentration (MIC) Data" (PDF). TOKU-E. Diarkibkan (PDF) daripada yang asal pada 2015-12-22. Dicapai pada 2014-03-31.
- ^ "Patch-test results of the North American Contact Dermatitis Group 2005-2006". Dermatitis. 20 (3): 149–60. 2009. doi:10.2310/6620.2009.08097. PMID 19470301. Unknown parameter
|displayauthors=ignored (bantuan) - ^ "Interaction of neuromuscular blocking effects of neomycin and polymyxin B". Anesthesiology. 50 (3): 218–20. March 1979. doi:10.1097/00000542-197903000-00010. PMID 219730.
- ^ "Neomycin and paromomycin inhibit 30S ribosomal subunit assembly in Staphylococcus aureus". Current Microbiology. 47 (3): 237–43. September 2003. doi:10.1007/s00284-002-3945-9. PMID 14570276.
- ^ "Binding of neomycin to phosphatidylinositol 4,5-bisphosphate (PIP2)". Biochimica et Biophysica Acta (BBA) - Biomembranes. 979 (1): 105–12. February 1989. doi:10.1016/0005-2736(89)90529-4. PMID 2537103.
- ^ "G418/neomycin-cross resistance?". Diarkibkan daripada yang asal pada 2009-06-25. Dicapai pada 2008-10-19.
- ^ "Neomycin—Production and Antibiotic Properties 123". The Journal of Clinical Investigation. 28 (5 Pt 1): 934–9. September 1949. doi:10.1172/JCI102182. PMC 438928. PMID 16695766.
- ^ Dewick M (March 2009). Medicinal natural products: a biosynthetic approach (ed. 3rd). The Atrium, Southern Gate, Chichester, West Sussex, United Kingdom: John Wiley and Sons Ltd. m/s. 508, 510, 511. ISBN 978-0-470-74168-9.
- ^ "Biosynthesis of 2-deoxystreptamine by three crucial enzymes in Streptomyces fradiae NBRC 12773". The Journal of Antibiotics. 58 (12): 766–74. December 2005. doi:10.1038/ja.2005.104. PMID 16506694.
- ^ "Discovery of parallel pathways of kanamycin biosynthesis allows antibiotic manipulation". Nature Chemical Biology. 7 (11): 843–52. October 2011. doi:10.1038/nchembio.671. PMID 21983602. Unknown parameter
|displayauthors=ignored (bantuan) - ^ "Unique O-ribosylation in the biosynthesis of butirosin". Bioorganic & Medicinal Chemistry. 15 (13): 4360–8. July 2007. doi:10.1016/j.bmc.2007.04.040. PMID 17482823.
- ^ "The neomycin biosynthetic gene cluster of Streptomyces fradiae NCIMB 8233: genetic and biochemical evidence for the roles of two glycosyltransferases and a deacetylase". Organic & Biomolecular Chemistry. 6 (18): 3306–14. September 2008. doi:10.1039/B808734B. PMID 18802637. Diarkibkan daripada yang asal pada 2021-03-18. Dicapai pada 2019-12-25.
- ^ "Biosynthesis of 2-deoxystreptamine-containing aminoglycoside antibiotics". Natural Product Reports. 23 (6): 864–74. December 2006. doi:10.1039/B604709M. PMID 17119636.
- ^ "Enzymatic preparation of neomycin C from ribostamycin". The Journal of Antibiotics. 62 (11): 643–6. November 2009. doi:10.1038/ja.2009.88. PMID 19713992.
- ^ Cammack R, Attwood TK, Campbell PN, Parish JH, Smith AD, Stirling JL, Vella F (2006). "neomycin". Oxford Dictionary of Biochemistry and Molecular Biology (ed. 2nd). Oxford University Press. m/s. 453.
- ^ "Comparative study of responses to neomycins B and C by microbiological and gas-liquid chromatographic assay methods". Applied Microbiology. 18 (3): 396–8. September 1969. doi:10.1128/AEM.18.3.396-398.1969. PMC 377991. PMID 4907002.
- ^ "Arginine-linked neomycin B dimers: synthesis, rRNA binding, and resistance enzyme activity". MedChemComm. 7 (1): 164–169. January 2016. doi:10.1039/C5MD00427F. PMC 4722958. PMID 26811742.
- ^ "Thermodynamics of aminoglycoside-rRNA recognition: the binding of neomycin-class aminoglycosides to the A site of 16S rRNA". Biochemistry. 41 (24): 7695–706. June 2002. doi:10.1021/bi020130f. PMID 12056901.
- ^ "DNA triple helix stabilization by aminoglycoside antibiotics". Bioorganic & Medicinal Chemistry Letters. 10 (17): 1897–9. September 2000. doi:10.1016/S0960-894X(00)00372-3. PMID 10987412.
- ^ "Neomycin-induced hybrid triplex formation". Journal of the American Chemical Society. 123 (44): 11093–4. November 2001. doi:10.1021/ja016481j. PMID 11686727.