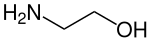
Etanolammina
L'etanolammina (o monoetanolammina, talvolta abbreviata in MEA, detta anche colammina) è un composto chimico che ha la funzione di ammina e di alcol.
| Etanolammina | |
|---|---|
 | |
| Nome IUPAC | |
| 2-amminoetanolo | |
| Caratteristiche generali | |
| Formula bruta o molecolare | NH2CH2CH2OH |
| Massa molecolare (u) | 61,08 g/mol |
| Aspetto | liquido incolore |
| Numero CAS | |
| Numero EINECS | 205-483-3 |
| PubChem | 700 |
| DrugBank | DBDB03994 |
| SMILES | C(CO)N |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,02 (20 °C) |
| Indice di rifrazione | 1,4539 |
| Solubilità in acqua | (20 °C) miscibile in ogni proporzione |
| Temperatura di fusione | 10 °C (283 K) |
| Temperatura di ebollizione | 171 °C (444 K) (1013 hPa) |
| Indicazioni di sicurezza | |
| Punto di fiamma | 95 °C (368 K) |
| Limiti di esplosione | 2,5 - 13,1 Vol% |
| Temperatura di autoignizione | 410 °C (683 K) |
| Simboli di rischio chimico | |
 
| |
| pericolo | |
| Frasi H | 302 - 312 - 332 - 314 - 335 |
| Consigli P | 261 - 280 - 305+351+338 - 308+313 [1] |
A temperatura ambiente si presenta come un liquido incolore dal lieve odore di ammoniaca. È un composto nocivo e irritante.
Produzione
modificaL'etanolammina viene prodotta industrialmente facendo reagire ossido di etilene con ammoniaca (a temperature comprese tra 60-150 °C e pressione di 30-150 bar):[2]
Come sottoprodotti (indesiderati) del processo di produzione di etanolammina si ottengono dietanolammina e trietanolammina, la cui concentrazione viene ridotta operando in eccesso di ammoniaca rispetto alla quantità stechiometrica.
Usi
modificaCome la DEA e la TEA, grazie al suo carattere basico, la MEA è utilizzata come soluzione assorbente per il recupero di sostanze acide, come ad esempio H2S ottenuto per idrodesolforazione del petrolio o del gas naturale.
Funzione biologica
modificaLegata ad un glicerofosfolipide dà la fosfatidiletanolammina, detta anche "cefalina". Quest'ultima ha funzione di trasporto degli acidi grassi e contribuisce al loro assorbimento a livello intestinale.
Interviene, in veste di nucleofilo, nella sostituzione nucleofila di tre molecole di S-adenosil metionina per produrre colina.
Note
modifica- ^ scheda del 2-amminoetanolo su IFA-GESTIS Archiviato il 16 ottobre 2019 in Internet Archive.
- ^ Weissermel-Arpe, p. 159.
Bibliografia
modifica- (EN) Klaus Weissermel, Hans-Jürgen Arpe, Charlet R. Lindley, Industrial organic chemistry, 4ª ed., Wiley-VCH, 2003, pp.159-161, ISBN 3-527-30578-5.
Altri progetti
modifica- Wikimedia Commons contiene immagini o altri file su etanolammina
Collegamenti esterni
modifica- (EN) ethanolamine, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.